Tresiba
Bula do Medicamento - Farmacologia do Remédio
Tresiba, para o que é indicado e para o que serve?
Tresiba ® ( insulina degludeca ) é indicado para o tratamento de diabetes mellitus em adultos, adolescentes e crianças acima de 1 ano de idade.
Tresiba ® pode ser usado em combinação com antidiabéticos orais, assim como com outras insulinas de ação rápida ou ultrarrápida.
Em pacientes com diabetes mellitus tipo 2, Tresiba ® pode ser utilizado isoladamente ou em combinação com antidiabéticos orais, agonistas de receptor de GLP-1 e insulina rápida ou ultrarrápida.
Em pacientes com diabetes mellitus tipo 1, Tresiba ® sempre deve ser administrado em combinação com insulina rápida ou ultrarrápida.
Como o Tresiba funciona?
Tresiba ® é uma insulina de ação ultralonga chamada insulina degludeca, usada para tratar diabetes mellitus em adultos, adolescentes e crianças acima de 1 ano. Tresiba ® ajuda seu corpo a reduzir o nível de açúcar no sangue (glicemia). É utilizado uma vez ao dia.
Em ocasiões em que você não pode aplicar no horário recomendado, você pode mudar o horário de aplicação, pois Tresiba ® tem um efeito prolongado na redução de açúcar no sangue.
Tresiba ® pode ser usado com insulina de ação rápida ou ultrarrápida. No diabetes mellitus tipo 2, Tresiba ® pode ser utilizado em combinação com antidiabéticos orais ou com outros antidiabéticos injetáveis que não a insulina. No diabetes mellitus tipo 1, Tresiba ® deve ser usado em combinação com insulinas de ação rápida ou ultrarrápida.
Exclusivo Tresiba ® Penfill ® 100 U/mL : Tresiba ® Penfill ® foi desenvolvido para ser utilizado com sistemas de aplicação de insulina da Novo Nordisk e agulhas descartáveis NovoFine ® . O seu médico pode pedir que use somente Tresiba ® ou Tresiba ® associado com outros medicamentos para diabetes.
Quais as contraindicações do Tresiba?
Não use Tresiba ® se você for alérgico (hipersensível) à insulina degludeca ou a qualquer um dos outros componentes do medicamento.
Como usar o Tresiba?
Tresiba ® FlexTouch ® 100 U/mL
Antes de usar Tresiba ® FlexTouch ® pela primeira vez, o seu médico ou profissional de saúde mostrará como usá-lo.
Verifique o nome e cor da etiqueta no sistema de aplicação para se certificar de que é Tresiba ® 100U/mL.
- Tresiba ® é administrado através de aplicação sob a pele (injeção subcutânea). Não injetá-lo na veia ou no músculo.
- Os melhores lugares para aplicar são a parte da frente das coxas, a parte superior dos braços ou a parte da frente da sua barriga (abdômen).
- Altere o local da injeção dentro da mesma região, a cada dia, para reduzir o risco de desenvolver caroços e lesões na pele.
- Sempre utilize uma agulha nova para cada injeção. A reutilização de agulhas pode aumentar o risco de agulhas entupidas, levando a uma dosagem imprecisa. Descarte a agulha com segurança após cada uso.
- Não use uma seringa para remover a solução do sistema de aplicação, para evitar erros de dosagem e potencial superdosagem.
Leia atentamente estas instruções antes de usar Tresiba ® FlexTouch ® .
Se você não seguir as instruções atentamente, você pode injetar muita ou pouca insulina, o que pode levar a níveis muito altos ou muito baixos de açúcar no sangue.
Não use seu sistema de aplicação sem a devida orientação do seu médico ou de outro profissional de saúde.
Comece verificando seu sistema de aplicação para certificar-se de que ele contém Tresiba ® 100U/mL, então veja as ilustrações abaixo para conhecer as diferentes partes de seu sistema de aplicação e agulha.
Se você é cego ou apresenta problemas visuais graves, não use este sistema de aplicação sem ajuda.
Obtenha ajuda de uma pessoa com boa visão, que seja treinada para usar o sistema de aplicação Tresiba ® FlexTouch ® .
Tresiba ® FlexTouch ® é um sistema de aplicação preenchido com insulina, com seletor de dose. Ele contém 300 unidades de insulina e proporciona doses de 1 a 80 unidades, em incrementos de 1 unidade. Não faça nenhum recálculo de dose. Tresiba ® FlexTouch ® pode ser administrado com agulhas descartáveis de até 8 mm de comprimento. Seu sistema de aplicação foi desenvolvido para ser utilizado com agulhas descartáveis NovoFine ® . As agulhas não estão incluídas na embalagem.
Informação importante
Preste atenção nestas informações para o uso correto da caneta.
Tresiba ® FlexTouch ® e agulha (exemplo):

Preparação do sistema de aplicação
- Verifique o nome e a cor da etiqueta do sistema de aplicação, para certificar-se de que ele contém Tresiba ® 100U/mL. Isto é especialmente importante se você usar mais de um tipo de insulina. Se você usar o tipo de insulina errado, seu nível de açúcar no sangue poderá ficar muito alto ou muito baixo;
- Retire a tampa do sistema de aplicação;
- Verifique se a insulina no sistema de aplicação está límpida e incolor. Olhe através do visor de insulina. Se a insulina parecer turva, não use o sistema de aplicação;
- Pegue uma nova agulha e retire o selo protetor;
- Encaixe a agulha no sistema de aplicação. Gire até que esteja firmemente acoplada;
- Retire a tampa externa da agulha e guarde-a. Você vai precisar dela após a injeção, para remover com segurança a agulha do sistema de aplicação.
- Retire a tampa interna da agulha e descarte-a. Se você tentar colocá-la novamente, você pode acidentalmente ferir-se com a agulha;
- Uma gota de insulina pode aparecer na ponta da agulha. Isso é normal, mas você ainda deve verificar o fluxo de insulina.
Utilize sempre uma agulha nova para cada injeção. Isso reduz o risco de contaminação, infecção, vazamento de insulina, agulhas entupidas e dosagem inadequada.
Nunca use uma agulha torta ou danificada.
Verificação do fluxo de insulina
- Sempre verifique o fluxo de insulina antes de começar. Isso ajuda você a garantir que obtenha sua dose completa de insulina;
- Gire o seletor de dose para selecionar 2 unidades. Certifique-se que o seletor de dose mostra 2.
- Segure o sistema de aplicação com a agulha apontando para cima. Bata levemente com o dedo no topo do sistema de aplicação algumas vezes para fazer com que qualquer bolha de ar suba para o topo;
- Pressione e segure o botão injetor até que o contador de dose mostre a dose “0” (zero). O “0” (zero) deve estar alinhado com o indicador de dose. Uma gota de insulina deve aparecer na ponta da agulha;
- Uma pequena bolha de ar pode permanecer na ponta da agulha, mas esta não será injetada. Se nenhuma gota aparecer, repita as etapas A à C até seis vezes. Se ainda não aparecer uma gota, mude a agulha e repita as etapas A à C mais uma vez. Se uma gota de insulina ainda não aparecer, descarte a caneta e use uma nova.
Certifique-se sempre de que uma gota apareça na ponta da agulha antes de injetar. Isso garante o fluxo de insulina. Se nenhuma gota aparecer, a insulina não será aplicada, mesmo que o contador de dose possa mover-se. Isto pode indicar agulhar bloqueada ou danificada.
Sempre verifique o fluxo antes de injetar. Se você não verificar o fluxo, você pode injetar muito pouca insulina ou nenhuma. Isto pode levar a um elevado nível de açúcar no sangue.
Seleção da sua dose
- Certifique-se de que o contador de dose está no “0” (zero) antes de começar. O “0” (zero) deve estar alinhado com o indicador da dose;
- Gire o seletor de dose para selecionar a dose que você precisa, como indicado pelo seu médico ou profissional de saúde. Se você selecionar uma dose errada, você pode girar o seletor de dose para frente ou para trás para corrigir a dose. A caneta pode selecionar até no máximo 80 unidades.
O seletor de dose altera o número de unidades. Apenas o contador de doses e o indicador de dose mostrarão quantas unidades você selecionou por dose.
Você pode selecionar até 80 unidades por dose. Quando a caneta contém menos de 80 unidades, o contador de dose para no número de unidades restantes.
O seletor de dose faz um clique diferente quando você gira para frente, para trás ou quando passa do número de unidades restantes. Não conte os cliques do sistema de aplicação.
Sempre use o contador de dose e o indicador de dose para ver quantas unidades você selecionou, antes de injetar a insulina. Não conte os cliques do sistema de aplicação. Se você selecionar e injetar a dose errada, seu nível de açúcar no sangue pode ficar muito baixo ou muito elevado. Não use a escala de insulina, pois esta apenas mostra aproximadamente quanto de insulina resta no sistema de aplicação.
Injetando a dose
- Insira a agulha sob a pele como o seu médico ou profissional de saúde orientou;
- Certifique-se de que você pode ver o contador de dose. Não cubra o contador de dose com os dedos. Isso pode interromper a injeção;
- Pressione e segure o botão de aplicação até que o contador mostre a dose “0” (zero). O “0” (zero) deve estar alinhado com o indicador de dose. Você poderá, então, ouvir ou sentir um clique;
- Deixe a agulha sob a pele durante pelo menos 6 segundos para ter certeza de que recebeu a dose completa;
- Retire a agulha da pele. Se aparecer sangue no local de injeção, pressione levemente com um cotonete. Não massageie a área;
- Você pode ver uma gota de insulina na ponta da agulha após a injeção. Isso é normal e não afeta a sua dose;
- Sempre observe o contador de dose para saber quantas unidades você injetará. O contador de dose mostra o número exato de unidades. Não conte pelos cliques do sistema de aplicação. . Nunca toque o contador de dose enquanto injeta. Isso pode interromper a injeção. Segure o botão de aplicação, após a injeção, até que o contador de dose volte a “0” (zero). Se o contador de dose parar antes que ele retorne para 0, a dose total não terá sido injetada, podendo resultar em alto nível de açúcar no sangue.
Após sua injeção
- Leve a ponta da agulha para dentro da tampa externa da agulha sobre uma superfície plana sem tocar na agulha ou na tampa externa da agulha.
- Quando a agulha estiver coberta, empurre cuidadosamente a tampa externa da agulha completamente ;
- Desrosque a agulha e descarte-a cuidadosamente;
- Coloque a tampa no sistema de aplicação após cada uso para proteger a insulina da luz;
Sempre descarte a agulha após cada injeção em um recipiente apropriado para objetos cortantes. Isso reduz o risco de contaminação, infecção, vazamento de insulina, agulhas entupidas e dosagem imprecisa. Se a agulha estiver entupida, você não conseguirá injetar a insulina.
Quando o sistema de aplicação estiver vazio, descarte-o sem agulha conforme indicado pelo seu médico ou profissional da saúde. Não descarte a agulha usada no lixo doméstico.
Nunca tente colocar a tampa interna da agulha de volta na agulha. Você pode se ferir com a agulha.
Sempre remova a agulha após cada injeção e guarde o sistema de aplicação sem a agulha rosqueada.
Isso reduz o risco de contaminação, infecção, vazamento de insulina, agulhas bloqueadas e dosagem imprecisa.
Qual a quantidade de insulina que resta?
- A escala de insulina mostra aproximadamente a quantidade de insulina restante no sistema de aplicação;
- Para ver a quantidade exata de insulina que resta, use o contador de dose:
Gire o seletor de dose até que o contador de dose pare.
Se ele mostrar 80, pelo menos 80 unidades restam no sistema de aplicação.
Se ele mostrar menos do que 80, o número mostrado é o número de unidades que restam no sistema de aplicação. - Gire o seletor de dose para trás até que o contador de dose mostre “0” (zero).
- Se você precisar de mais insulina do que as unidades restantes no sistema de aplicação, você pode dividir a sua dose entre dois sistemas de aplicação.
Tenha muito cuidado para calcular corretamente se você dividir a dose. Em caso de dúvida, aplique a dose completa com um novo sistema de aplicação. Se você injetar a dose errada, você injetará muito pouco ou muita insulina, que pode levar a um nível muito alto ou muito baixo de açúcar no sangue.
Importante
- Mantenha sempre o sistema de aplicação com você.
- Leve sempre um sistema de aplicação extra e novas agulhas com você, em caso de perda ou dano.
- Mantenha sempre o sistema de aplicação e agulhas fora da vista e do alcance de outras pessoas, especialmente crianças.
- Nunca compartilhe o sistema de aplicação ou as suas agulhas com outras pessoas. Isto pode levar a uma infecção cruzada.
- Nunca compartilhe o sistema de aplicação ou as suas agulhas com outras pessoas. Seu medicamento pode ser prejudicial à saúde delas.
- Os cuidadores devem ser muito cautelosos ao manusear agulhas usadas - para reduzir o risco de lesões com as agulha e infecção cruzada.
Cuidado com seu sistema de aplicação
Cuide do seu sistema de aplicação. O mau uso pode gerar uma dose imprecisa, levando a um nível de açúcar no sangue muito baixo ou muito alto.
- Não o deixe dentro do carro ou outro lugar onde ele possa ficar muito quente ou muito frio.
- Não exponha o sistema de aplicação à sujeira, pó ou líquido.
- Não lave, molhe ou lubrifique o sistema de aplicação. Se necessário, limpe-o com detergente neutro em um pano umedecido.
- Não deixe seu sistema de aplicação cair ou bater contra superfícies duras. Se você deixá-lo cair ou suspeitar de um problema, rosqueie uma nova agulha e verifique o fluxo de insulina antes de injetar.
- Não tente recarregar o sistema de aplicação. Uma vez vazio, ele deve ser descartado.
- Não tente reparar o sistema de aplicação ou desmontá-lo.
- Para armazenar o sistema de aplicação, veja item Como devo armazenar o Tresiba?
Sempre use este medicamento exatamente como o seu médico indicou. Caso você não tenha certeza de como utilizá-lo, consulte seu médico ou outro profissional de saúde.
Cegos ou pessoas que apresentam problemas visuais e não podem ler o contador de dose da caneta, não devem usar o sistema de aplicação sem ajuda. Solicite ajuda de uma pessoa com boa visão e treinada para usar o sistema de aplicação Tresiba ® FlexTouch ® .
Tresiba ® FlexTouch ® 100 U/mL pode dispensar doses de 1-80 unidades por injeção, em incrementos de 1 unidade. O contador de doses do sistema de aplicação mostra o número de unidades de insulina a serem injetadas. Não faça qualquer recálculo de dose.
Dosagem
Você e seu médico decidirão:
- Quanto Tresiba ® você vai precisar por dia;
- Quando verificar o nível de açúcar no sangue e se você precisa de uma dose maior ou menor.
Tresiba ® pode ser usado com insulina de ação rápida ou ultrarrápida. No diabetes mellitus tipo 2, Tresiba ® pode ser utilizado em combinação com antidiabéticos orais ou com outros antidiabéticos injetáveis que não a insulina. No diabetes mellitus tipo 1, Tresiba ® deve ser usado em combinação com insulinas de ação rápida ou ultrarrápida.
Flexibilidade do horário de aplicação
- Siga sempre a recomendação de dose do seu médico.
- Use Tresiba ® uma vez ao dia, preferencialmente no mesmo horário todos os dias.
- Em ocasiões quando não for possível usar Tresiba ® no mesmo horário do dia, é possível aplicar em outro horário do dia. Assegure-se de haver no mínimo 8 horas entre as aplicações. Não há experiência com flexibilidade no horário de administração de Tresiba ® em crianças e adolescentes.
- Se você quiser mudar a sua dieta habitual, verifique antes com seu médico ou outro profissional de saúde, visto que uma alteração na dieta pode alterar suas necessidades de insulina.
O seu médico pode alterar a sua dose com base no seu nível de açúcar no sangue.
Quando usar outros medicamentos, pergunte ao seu médico se o seu tratamento precisa ser ajustado.
Não use Tresiba ® FlexTouch ®
- Em bombas de infusão de insulina.
- Se o sistema de aplicação estiver danificado ou não foi corretamente armazenado.
- Se a insulina não tiver aspecto límpido e incolor.
Uso em crianças e adolescentes
- Tresiba ® pode ser usado em adolescentes e crianças acima de 1 ano de idade. Não existe experiência com o uso de Tresiba ® em crianças menores de 1 ano de idade.
Uso em idosos (≥ 65 anos)
- Tresiba ® pode ser usado por pacientes idosos, mas você talvez precise verificar seu nível de açúcar no sangue mais regularmente. Converse com o seu médico sobre as mudanças na sua dose. Converse com o seu médico sobre as mudanças na sua dose.
Se você tiver problemas nos rins ou no fígado
- Se você tiver problemas nos rins ou no fígado pode ser necessário verificar o seu nível de açúcar no sangue mais regularmente. Converse com seu médico sobre as mudanças na sua dose de Tresiba ® .
Se você parar de usar Tresiba ®
Não pare de utilizar sua insulina sem falar com seu médico. Se você parar de utilizar sua insulina, seu nível de açúcar no sangue pode aumentar muito e levar à cetoacidose (uma condição em que o sangue fica mais ácido do que o normal)
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
Tresiba ® Penfill 100 U/mL
Sempre use este medicamento exatamente como o seu médico indicou. Caso você não tenha certeza de como utilizá-lo, consulte seu médico ou profissional de saúde.
Cegos ou pessoas que apresentam problemas visuais e não podem ler o contador de dose da caneta, não devem usar o sistema de aplicação sem ajuda. Solicite ajuda de uma pessoa com boa visão e treinada para usar o sistema de aplicação.
Antes de usar Tresiba ® Penfill ® pela primeira vez, o seu médico ou profissional de saúde mostrará como usá-lo.
Por favor, leia também o manual que vem com seu sistema de aplicação de insulina.
Verifique o nome e a cor da etiqueta na caneta para se certificar de que é Tresiba ® 100U/mL.
- Tresiba ® é administrado através de aplicação sob a pele (injeção subcutânea). Não injetá-lo na veia ou no músculo.
- Os melhores lugares para aplicar são a parte da frente das coxas, a parte superior dos braços ou a parte da frente da sua barriga (abdômen).
- Altere o local da injeção dentro da mesma região, a cada dia, para reduzir o risco de desenvolver caroços e lesões na pele.
- Sempre utilize uma agulha nova para cada injeção. A reutilização de agulhas pode aumentar o risco de agulhas entupidas, levando a uma dosagem imprecisa. Descarte a agulha com segurança após cada uso.
- Não use uma seringa para remover a solução da caneta, para evitar erros de dose e potencial overdose.
Dosagem
Você e seu médico decidirão:
- Quanto Tresiba ® você vai precisar por dia;
- Quando verificar o nível de açúcar no sangue e se você precisa de uma dose maior ou menor.
Tresiba ® pode ser usado com insulina de ação rápida ou ultrarrápida. No diabetes mellitus tipo 2, Tresiba ® pode ser utilizado em combinação com antidiabéticos orais ou com outros antidiabéticos injetáveis que não a insulina. No diabetes mellitus tipo 1, Tresiba ® deve ser usado em combinação com insulinas de ação rápida ou ultrarrápida.
Flexibilidade do horário de aplicação
- Siga sempre a recomendação de dose do seu médico.
- Use Tresiba ® uma vez ao dia, preferencialmente no mesmo horário todos os dias.
- Em ocasiões quando não for possível usar Tresiba ® no mesmo horário do dia, é possível aplicar em outro horário do dia. Assegure-se de haver no mínimo 8 horas entre as aplicações. Não há experiência com flexibilidade no horário de administração de Tresiba ® em crianças e adolescentes.
- Se você quiser mudar a sua dieta habitual, verifique antes com seu médico ou outro profissional de saúde, visto que uma alteração na dieta pode alterar suas necessidades de insulina.
O seu médico pode alterar a sua dose com base no seu nível de açúcar no sangue.
Quando usar outros medicamentos, pergunte ao seu médico se o seu tratamento precisa ser ajustado.
Não use Tresiba ® Penfill ®
- Em bombas de infusão de insulina.
- Se Tresiba ® Penfill ® ou o sistema de aplicação que você está utilizando estiver danificado. Veja o manual do sistema de aplicação para outras instruções.
- Se Tresiba ® Penfill ® estiver danificado ou não foi corretamente armazenado.
- Se a insulina não tiver aspecto límpido e incolor.
Uso em crianças e adolescentes
- Tresiba ® pode ser usado em adolescentes e crianças acima de 1 ano de idade. Não existe experiência com o uso de Tresiba ® em crianças menores de 1 ano de idade.
- Em crianças, deve-se tomar cuidado para que as doses de insulina (especialmente em regime basal-bolus) coincidam com a ingestão de alimentos e a realização de atividades físicas, a fim de minimizar o risco de hipoglicemia .
- Não há experiência clínica do uso da insulina degludeca em crianças e adolescentes de até 18 anos de idade com diabetes mellitus do tipo 2. Os dados para adolescentes com diabetes mellitus do tipo 2 foram extrapolados.
Uso em idosos (≥ 65 anos)
- Tresiba ® pode ser usado por pacientes idosos, mas você pode precisar verificar seu nível de açúcar no sangue mais regularmente. Converse com o seu médico sobre as mudanças na sua dose.
Se você tiver problemas nos rins ou no fígado
- Se você tiver problemas nos rins ou no fígado pode ser necessário verificar o seu nível de açúcar no sangue mais regularmente. Converse com seu médico sobre as mudanças na sua dose de Tresiba ® .
Se você parar de usar Tresiba ®
Não pare de utilizar sua insulina sem falar com seu médico. Se você parar de utilizar sua insulina, isto pode aumentar muito seu nível de açúcar no sangue e levar à cetoacidose (uma condição em que o sangue fica mais ácido do que o normal).
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O que eu devo fazer quando esquecer de usar o Tresiba?
Se você esquecer uma dose, tome a dose esquecida assim que perceber garantindo um mínimo de 8 horas entre as doses. Caso você perceba que se esqueceu de tomar a dose anterior no momento de tomar a dose atual não tome uma dose dupla e retorne a sua dose diária habitual.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Quais cuidados devo ter ao usar o Tresiba?
Leia toda a bula com atenção antes de começar a usar este medicamento, pois contem informações importantes para você.
- Mantenha esta bula com você. Você pode precisar lê-la novamente.
- Se você tiver dúvidas adicionais, pergunte ao seu médico ou profissional de saúde.
- Este medicamento foi prescrito apenas para você. Não o dê para outras pessoas.
- Ele poderá causar danos até mesmo se os sinais da doença forem os mesmos que os seus.
- Se você apresentar qualquer efeito adverso converse com o seu médico ou profissional de saúde. Isto inclui qualquer possível efeito adverso não mencionado nesta bula.
Converse com seu médico ou profissional de saúde antes de usar Tresiba ® .
Tenha especial atenção nos seguintes casos:
- Baixo nível de açúcar no sangue (hipoglicemia) – se o seu nível de açúcar no sangue estiver muito baixo, siga a orientação para baixo nível de açúcar no sangue, descrito no item Quais as reações adversas e os efeitos colaterais do Tresiba? ”.
- Alto nível de açúcar no sangue ( hiperglicemia ) – se o seu nível de açúcar no sangue está muito alto, siga a orientação para alto nível de açúcar no sangue, descrito no item Quais as reações adversas e os efeitos colaterais do Tresiba? .
- Transferência de outro tipo de insulina – a dose de insulina pode precisar ser alterada se você mudar de marca ou fabricante de insulina. Converse com seu médico.
- Tiazolidinedionas usadas em combinação com insulina, vide item “tiazolidinedionas”.
- Distúrbio visual – a rápida melhora no controle do açúcar no sangue pode levar a piora temporária do distúrbio visual diabético. Se você apresentar problemas visuais, converse com seu médico.
- Garanta que você está usando o tipo certo de insulina – sempre verifique o rótulo da insulina antes de cada injeção para evitar a troca acidental de Tresiba ® com outras insulinas.
Para pacientes com deficiência visual, verificar o item “ Como usar o Tresiba? ”.
Alterações da pele no local da injeção
O local da injeção deve ser alternado para ajudar a prevenir alterações no tecido adiposo sob a pele, tais como espessamento da pele, encolhimento da pele ou caroços sob a pele. A insulina pode não funcionar muito bem se você injetar em uma área irregular, encolhida ou mais espessa. Informe o seu médico se você detectar quaisquer alterações da pele no local da injeção. Informe o seu médico se atualmente você estiver injetando nessas áreas afetadas antes de começar a injetar em uma área diferente. O seu médico pode pedir-lhe para verificar mais frequentemente o nível de açúcar no sangue e ajustar a dose de insulina ou de outros medicamentos antidiabéticos.
Crianças e adolescentes
Tresiba ® pode ser usado por adolescentes ou crianças acima de 1 ano de idade. Não existe experiência com o uso de Tresiba ® em crianças menores de 1 ano de idade.
Em crianças, deve-se tomar cuidado para que as doses de insulina (especialmente em regime basal-bolus) coincidam com a ingestão de alimentos e a realização de atividades físicas, a fim de minimizar o risco de hipoglicemia.
Não há experiência clínica do uso da insulina degludeca em crianças e adolescentes de até 18 anos de idade com diabetes mellitus tipo 2. Os dados para adolescentes com diabetes mellitus do tipo 2 foram extrapolados.
Gravidez e Amamentação
Não se sabe se Tresiba ® afeta o bebê na gestação ou durante a amamentação. Fale com o seu médico para aconselhamento antes de usar este medicamento, se você estiver grávida, achar que pode estar grávida, planejando engravidar ou amamentando. Sua dose de insulina pode necessitar de ajuste durante a gravidez e após o parto. É necessário um controle cuidadoso do seu diabetes durante a gravidez. É importante para a saúde de seu bebê evitar níveis muito baixos de açúcar no sangue (hipoglicemia).
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Dirigindo e usando máquinas
Níveis muito baixos (hipoglicemia) ou muito altos (hiperglicemia) de açúcar no sangue podem afetar sua capacidade de dirigir ou utilizar quaisquer ferramentas ou máquinas. Se seu nível de açúcar no sangue está muito alto ou muito baixo, sua habilidade para concentrar-se ou reagir pode estar afetada. Isto pode ser perigoso para você e para os outros.
Consulte seu médico para saber se você pode dirigir:
- Frequentemente fica com o nível de açúcar no sangue muito baixo;
- Acha difícil reconhecer quando o nível de açúcar no sangue está muito baixo.
Importante informação sobre alguns componentes de Tresiba ®
Tresiba ® contém menos de 23 mg (1 mmol) de sódio por dose. Isto significa que Tresiba ® é essencialmente "livre de sódio".
Este medicamento pode causar doping.
Quais as reações adversas e os efeitos colaterais do Tresiba?
Como os demais medicamentos, Tresiba ® pode causar efeitos colaterais, embora nem todos os pacientes os apresentem:
Alterações da pele no local da injeção
- Se você injetar insulina no mesmo local, o tecido adiposo pode encolher (lipoatrofia) ou ficar mais espesso (lipohipertrofia) (podem ocorrer em até 1 em 100 pessoas). Caroços sob a pele também podem ser causados pelo acúmulo de uma proteína chamada amilóide ( amiloidose cutânea; a frequência com que isso ocorre é desconhecida). A insulina pode não funcionar muito bem se você injetar em uma área irregular, encolhida ou mais espessa. Alterne o local da injeção a cada aplicação para ajudar a prevenir essas alterações na pele.
Reação muito comum (pode ocorrer em mais 1 em 10 pacientes)
- Hipoglicemia (nível muito baixo de açúcar no sangue), que pode ser muito grave. Se seu nível de açúcar no sangue diminuir demais você pode ficar inconsciente. Hipoglicemia grave pode causar dano cerebral e pode ser fatal. Se você tiver sintomas de baixo nível de açúcar no sangue, tome ações para aumentar o nível de açúcar no sangue imediatamente.
Reação comum (pode ocorrer em até 1 em 10 pacientes)
Reações locais
Pode ocorrer reação no local de aplicação.
Os sinais podem incluir:
- Dor, vermelhidão, urticária , inchaço e coceira. As reações geralmente desaparecem depois de alguns dias. Consulte o seu médico se não desaparecerem após algumas semanas. Pare de usar Tresiba ® e consulte um médico imediatamente caso as reações se tornem graves.
Reações incomuns (pode ocorrer em até 1 em 100 pacientes)
Inchaço ao redor das suas articulações
- Quando você começa a utilizar o medicamento, seu corpo pode reter mais água do que deveria. Isso pode causar inchaço ao redor dos tornozelos e outras articulações. Isto geralmente é de curta duração.
Reações raras (pode ocorrer em até 1 em 1000 pacientes)
- Este medicamento pode causar reações alérgicas tais como urticária, inchaço da língua e dos lábios, diarréia, cansaço , náuseas e coceira.
Reação alérgica grave
Reação alérgica grave: se você tiver uma reação alérgica grave ao Tresiba ® ou a qualquer um de seus componentes, pare de usar Tresiba ® e consulte um médico imediatamente.
Os sinais de uma reação alérgica grave são:
- As reações locais espalham para outras partes do seu corpo;
- Você de repente se sente mal e transpira;
- Você começar a apresentar vômitos ;
- Você sente dificuldade em respirar;
- Você apresenta batimento cardíaco rápido ou sensação de tontura .
Outros efeitos do tratamento do diabetes
Nível muito baixo de açúcar no sangue (hipoglicemia)
Nível muito baixo de açúcar no sangue pode ocorrer se você:
- Tomar bebidas alcoólicas; usar muita insulina; exercitar-se mais do que o normal; comer muito pouco ou pular uma refeição.
Sinais de alerta de nível muito baixo de açúcar no sangue - estes podem surgir rapidamente:
- Dor de cabeça , fala arrastada, batimento cardíaco acelerado, suor frio, pele fria e pálida, sentir-se adoentado, sentir muita fome, tremor ou sensação de nervoso ou preocupação, sentir um cansaço anormal, fraqueza e sonolência, sensação de confusão, dificuldade de concentração, mudanças de curta duração na sua visão.
O que fazer se você apresentar níveis muito baixos de açúcar no sangue
- Coma açúcar ou outro alimento muito açucarado como doces, biscoitos ou suco de fruta (sempre leve açúcar ou alimento muito açucarado, por precaução).
- Se possível dose o açúcar no sangue e descanse. Você pode precisar medir o açúcar no sangue mais de uma vez, visto que com toda insulina basal a melhora pode demorar.
- Aguarde até que os sinais de baixo nível de açúcar no sangue tenham desaparecido ou que o seu nível de açúcar no sangue se restabeleça. Em seguida, continue com a sua insulina, como de costume.
O que os outros precisam fazer caso você desmaie:
- Informe que você tem diabetes a todos com quem você passa mais tempo. Informe a eles o que pode acontecer, incluindo o risco de desmaiar quando o nível de açúcar no sangue ficar muito baixo.
Eles devem saber que, se você desmaiar, eles devem:
- Virar você de lado;
- Obter ajuda médica imediatamente;
- Não dar a você nada para comer ou beber, pois você poderá engasgar.
Você pode se recuperar mais rapidamente do desmaio com uma injeção de glucagon . Esta só pode ser administrada por alguém que saiba como usá-la.
- Se você receber glucagon, você vai precisar de açúcar ou um alimento açucarado assim que você se recuperar;
- Se você não responder a uma injeção de glucagon, você terá que ser tratado em um hospital;
- Se a hipoglicemia grave não for tratada ao longo do tempo, pode ocorrer dano cerebral. Isto pode ser de curta ou longa duração e pode levar à morte.
Converse com seu médico se:
- O nível de açúcar no sangue ficou tão baixo que você desmaiou;
- Você usou uma injeção de glucagon;
- Você apresentou hipoglicemia algumas vezes recentemente. Isso pode acontecer porque a dose ou o horário de suas aplicações de insulina, alimentação ou exercício podem precisar ser alterados.
Nível muito alto de açúcar no sangue (hiperglicemia)
Nível muito alto de açúcar no sangue pode acontecer se você:
- Comer mais ou se exercitar menos do que o habitual; tomar bebida alcoólica; tiver uma infecção ou febre ; não usar insulina suficiente; usar constantemente menos insulina do que você precisa; esquecer de usar a sua insulina ou parar de usar a insulina sem falar com seu médico.
Sinais de alerta de nível muito alto de açúcar no sangue - estes normalmente aparecem gradualmente:
- Vermelhidão da pele, pele seca , sonolência ou cansaço; boca seca, respiração com odor de fruta (hálito cetônico); urinar com mais frequência, sensação de sede; perda de apetite, mal-estar (náuseas ou vômitos).
- Estes podem ser sinais de uma condição muito grave chamada cetoacidose. Este é um acúmulo de ácido no sangue porque o corpo está utilizando a gordura em vez de açúcar. Se não for tratada, esta pode levar ao coma diabético e eventualmente à morte.
O que fazer se você apresentar nível muito alto de açúcar no sangue:
- Teste seu nível de açúcar no sangue;
- Se puder, teste sua urina para cetonas;
- Obtenha ajuda médica imediatamente.
Se você apresentar qualquer efeito colateral, fale com o seu médico ou profissional de saúde. Isto inclui quaisquer possíveis efeitos colaterais não mencionados nesta bula.
Atenção: este produto é um medicamento que possui nova indicação terapêutica no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico.
Apresentações do Tresiba
Tresiba ® FlexTouch ® 100 U/mL
Embalagens com 1 ou 5 sistema(s) de aplicação preenchido(s), cada um com 3 mL de solução injetável de insulina degludeca.
Via subcutânea.
Uso adulto e pediátrico acima de 1 ano.
Tresiba ® Penfill ® 100 U/mL
Embalagens com 5 carpules, cada um com 3 mL de solução injetável de insulina degludeca.
Via subcutânea.
Uso adulto e pediátrico acima de 1 ano.
Qual a composição do Tresiba?
Tresiba ® FlexTouch ® 100 U/mL
1 mL de solução contém:
100 U (equivalente a 3,66 mg de insulina degludeca) de insulina degludeca.
Excipientes: glicerol , metacresol, fenol, acetato de zinco , ácido clorídrico, hidróxido de sódio e água para injetáveis .
Cada sistema de aplicação preenchido de Tresiba ® FlexTouch ® contém 3 mL equivalente a 300 U. Uma unidade (U) de insulina degludeca corresponde a uma unidade internacional (UI).
O sistema de aplicação preenchido pode fornecer uma dose máxima de 80 unidades em uma única injeção com incrementos de dose de 1 unidade.
A insulina degludeca é produzida por tecnologia do DNA recombinante em Saccharomyces cerevisiae .
Tresiba ® Penfill ® 100 U/mL
1 mL de solução contém:
100 U (equivalente a 3,66 mg de insulina degludeca) de insulina degludeca.
Excipientes: glicerol, metacresol, fenol, acetato de zinco, ácido clorídrico, hidróxido de sódio e água para injetáveis.
Cada carpule de Tresiba ® Penfill ® contém 3 mL equivalente a 300 U. Uma unidade (U) de insulina degludeca corresponde a uma unidade internacional (UI).
A insulina degludeca é produzida por tecnologia do DNA recombinante em Saccharomyces cerevisiae.
Superdose: o que acontece se tomar uma dose do Tresiba maior do que a recomendada?
Se você usar muita insulina o seu açúcar no sangue pode ficar muito baixo (hipoglicemia).
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação medicamentosa: quais os efeitos de tomar Tresiba com outros remédios?
Informe ao seu médico ou outro profissional de saúde se você estiver tomando ou tiver tomado recentemente qualquer outro medicamento, incluindo medicamentos obtidos sem receita médica.
Alguns medicamentos afetam o seu nível de açúcar no sangue, isso pode significar que sua dose de insulina precise mudar.
Os medicamentos mais comuns que podem afetar o seu tratamento com insulina estão listados a seguir:
Seu nível de açúcar no sangue pode diminuir (hipoglicemia), se você utilizar:
- Outros medicamentos para diabetes (oral ou injetável);
- Sulfonamidas - para infecções;
- Esteroides anabolizantes - como a testosterona ;
- Betabloqueadores - para pressão alta . Eles podem tornar mais difícil de reconhecer os sinais de nível muito baixo de açúcar no sangue;
- Ácido acetilsalicílico (e outros salicilatos) - para dor e febre baixa;
- Inibidores da monoaminoxidase (IMAO) - para depressão ;
- Inibidores da enzima conversora da angiotensina (ECA) - para alguns problemas cardíacos ou pressão alta.
Seu nível de açúcar no sangue pode aumentar (hiperglicemia), se você utilizar:
- Danazol - para endometriose ;
- Contraceptivos orais - pílula anticoncepcional ;
- Hormônios da tireoide - para problemas de tireoide;
- Hormônio do crescimento - para deficiência de hormônio de crescimento;
- Glicocorticoides como a cortisona - para a inflamação;
- Simpatomiméticos como a epinefrina (adrenalina), salbutamol ou terbutalina - para asma ;
- Tiazidas - para pressão alta ou se o seu corpo está acumulando muita água (retenção de líquidos).
Octreotida e lanreotida
Usado para o tratamento de uma condição rara envolvendo excesso de hormônio do crescimento ( acromegalia ). Ambos podem aumentar ou diminuir o seu nível de açúcar no sangue.
Tiazolidinediona
Medicamento antidiabético oral utilizado para o tratamento do diabetes mellitus tipo 2: alguns pacientes com diabetes mellitus tipo 2 de longa data e doença cardíaca ou acidente vascular cerebral prévio, que foram tratados com tiazolidinediona e insulina, desenvolveram insuficiência cardíaca . Informe o seu médico o mais rápido possível se você apresentar sinais de insuficiência cardíaca, tais como falta de ar incomum, ou aumento rápido do peso ou inchaço localizado ( edema ).
Se alguma das situações acima se aplica a você (ou você não tem certeza), fale com seu médico ou profissional de saúde.
Tresiba ® com álcool
Se você tomar bebidas alcoólicas, sua necessidade de insulina pode mudar. Seu nível de açúcar no sangue pode tanto diminuir quanto aumentar. Por isso, seu nível de açúcar no sangue deverá ser monitorado mais frequentemente do que o usual.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Interação alimentícia: posso usar o Tresiba com alimentos?
O álcool pode intensificar ou diminuir o efeito hipoglicêmico da insulina.
Qual a ação da substância do Tresiba (Insulina Degludeca)?
Resultados de Eficácia
Foram realizados 11 estudos clínicos, treat to target (com tratamento para meta glicêmica estabelecida), multinacionais, abertos, controlados, randomizados, paralelos, com duração de 26 ou 52 semanas, expondo 4275 pacientes à Insulina Degludeca (1102 com diabetes mellitus tipo 1 e 3173 com diabetes mellitus tipo 2).
A eficácia e segurança foram confirmadas com dose única diária de Insulina Degludeca, na mesma hora do dia e em horários flexíveis tanto para o início quanto na intensificação da insulinoterapia.
Insulina Degludeca melhora efetivamente o controle glicêmico conforme avaliado pela HbA1c. Foi confirmada não-inferioridade na alteração da HbA1c do início até o final do estudo tratando o paciente para o alvo estabelecido de glicemia em todos os estudos contra todos os comparadores, exceto contra sitagliptina, onde a Insulina Degludeca foi significativamente superior. A não inferioridade da HbA1c foi também confirmada para aplicação no mesmo período do dia e em esquemas de horário de aplicação flexíveis em portadores de diabetes tipos 1 e 2. 1, 2, 3, 4, 5, 6, 7, 8
Nos estudos treat to target em pacientes com diabetes mellitus tipo 1 e tipo 2, Insulina Degludeca forneceu o mesmo nível de controle glicêmico enquanto manteve a redução do risco de hipoglicemia nas 24 horas, quando o horário da aplicação é alterado de um dia para outro em comparação com a administração no mesmo horário todos os dias. 4, 8
Insulina Degludeca reduz a glicemia de jejum mais do que a insulina glargina em pacientes com diabetes mellitus tipo 1 e tipo 2, mais do que a insulina detemir em pacientes com diabetes mellitus tipo 1 e mais do que a sitagliptina em pacientes com diabetes mellitus tipo 2.
No diabetes mellitus tipo 2 um estudo clínico treat to target envolvendo pacientes em início da insulinoterapia mostrou uma taxa de hipoglicemia noturna confirmada 36% menor (definida como episódios entre a meia-noite e as seis horas da manhã, confirmada pela glicemia < 54 mg/dL (3,1 mmol/L) ou pelo paciente necessitar de assistência de outra pessoa) com Insulina Degludeca uma vez ao dia em comparação com a insulina glargina, ambos em combinação com antidiabéticos orais (ADO). Em um estudo clínico treat to target, que avaliou a terapia basal/ bolus em pacientes com diabetes mellitus tipo 2, Insulina Degludeca mostrou uma redução no risco de hipoglicemia nas 24 horas e noturna em comparação com a insulina glargina 1,2.
Episódios de hipoglicemia confirmados
Figura 1. Episódios de hipoglicemia confirmados e episódios de hipoglicemia noturna confirmados – Relacionados ao tratamento – Função cumulativa média. Diabetes mellitus tipo 2 em estudo de 52 semanas com insulina basal e antidiabéticos orais:
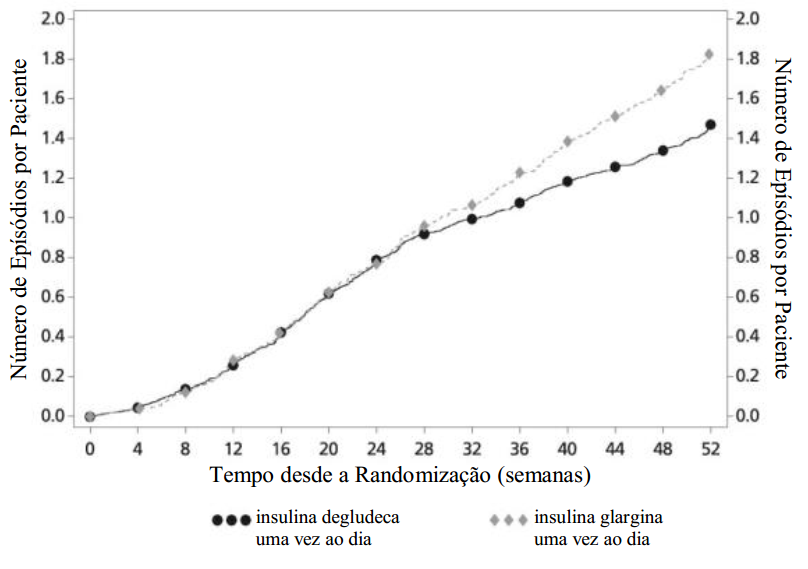
E pisódios de hipoglicemia noturna confirmados

Período noturno: período entre 00:01 e 05:59 da manhã (ambos incluídos).
Episódios de hipoglicemia confirmados
Figura 2. Episódios de hipoglicemia confirmados (A) e episódios de hipoglicemia noturna confirmados (B) – Relacionados ao tratamento - Função cumulativa média - diabetes mellitus tipo 2 em estudo de 52 semanas com antidiabéticos orais e insulinoterapia basal- bolus :

Episódios de hipoglicemia noturna confirmados

Período noturno: período entre 00:01 e 05:59 da manhã (ambos incluídos).
Os estudos clínicos treat to target com pacientes com diabetes mellitus tipo 1 com Insulina Degludeca versus insulina detemir e versus insulina glargina, mostraram taxas de hipoglicemia noturna confirmada para Insulina Degludeca 34% e 25% inferiores, respectivamente. 6,7,8
Em uma meta-análise prospectivamente planejada com sete estudos treat to target, em pacientes com diabetes mellitus tipo 1 e tipo 2, Insulina Degludeca foi superior em termos de menor número de episódios de hipoglicemia confirmados relacionados ao tratamento e episódios hipoglicêmicos noturnos confirmados comparado com a insulina glargina. Os resultados demonstram que o nível mais baixo da glicose plasmática de jejum com Insulina Degludeca é atingido com um menor risco de hipoglicemia. No período de manutenção, os benefícios observados tornaram-se mais pronunciados, refletindo uma redução sustentada ou ainda maior no risco de hipoglicemia ao longo do tempo com Insulina Degludeca uma vez ao dia em comparação com a insulina glargina uma vez ao dia. 1,2,3,4,6,8,9
Tabela 1. Desfechos da meta-análise de hipoglicemia:
| - | Hipoglicemia confirmada a | |
| Razão estimada de tratamento (Insulina Degludeca/ insulina glargina) | Total (nas 24 horas) | Noturna |
| Diabetes mellitus tipo 1 + tipo 2 (agrupados) | 0,91* | 0,74* |
| Período de manutenção* b | 0,84* | 0,68* |
| Indivíduos geriátricos ≥ 65 anos | 0,82 | 0,65* |
| Diabetes mellitus tipo 1 | 1,10 | 0,83 |
| Período de manutenção* b | 1,02 | 0,75* |
| Diabetes mellitus tipo 2 | 0,83* | 0,68* |
| Período de manutenção* b | 0,75* | 0,62* |
| Terapia basal isolada em pacientes sem uso prévio de insulina | 0,83* | 0,64* |
*Estatisticamente significante.
a Hipoglicemia confirmada foi definida como episódios confirmados de glicemia plasmática <3.1mmol/Lou paciente necessitando de assistência de terceiros. Hipoglicemia noturna confirmada foi definida como aquela que ocorreu da 00:01h às 5:59h.
b episódios a partir da semana 16.
Não há desenvolvimento clínico relevante de anticorpos anti-insulina após tratamento de longo prazo com Insulina Degludeca.
(Em um estudo clínico de 104 semanas, 57% dos pacientes com diabetes tipo 2 tratados com Insulina Degludeca (Insulina Degludeca) em combinação com metformina atingiu um alvo HbA1c <7,0%, e os pacientes remanescentes continuaram em um estudo clínico aberto de 26 semanas e foram randomizados para adicionar ao tratamento liraglutida ou uma única dose de insulina asparte (na refeição principal). No braço de Insulina Degludeca + liraglutida, a dose de insulina foi reduzida em 20%, a fim de minimizar o risco de hipoglicemia. A adição de liraglutida resultou em uma redução estatística em uma maior redução da HbA1c (-0,73% para – liraglutida vs 0,40% por comparador médias estimadas) e peso corporal (-3,03 vs 0,72 kg). A taxa de episódios hipoglicémicos (paciente por ano de exposição) foi estatisticamente e significativamente inferior ao adicionar liraglutida em comparação com a adição de uma única dose de insulina asparte (1,0 vs 8,15; proporção: 0,13; IC 95%: 0,08 0,21).
População pediátrica 10
A eficácia e segurança da Insulina Degludeca foram estudadas em um estudo clínico randomizado controlado 1:1, em crianças e adolescentes com diabetes mellitus tipo 1, por um período de 26 semanas (n = 350), seguido por um período de extensão de 26 semanas (n = 280). O braço de pacientes do Insulina Degludeca incluiu 43 crianças com idade entre 1-5 anos, 70 crianças com idade entre 6-11 anos e 61 dolescentes com idades entre 12-17 anos. Insulina Degludeca administrado uma vez por dia mostrou uma redução similar em HbA1c na semana 52 e maior redução na FPG da linha de base em relação ao comparador insulina detemir administrado uma vez ou duas vezes por dia. Isto foi atingido com 30% de doses diária a menos de Insulina Degludeca em comparação com a insulina detemir. As taxas (eventos por paciente por ano de exposição) de hipoglicemia grave (definição ISPAD; 0,51 vs 0,33), hipoglicemia confirmada (57,71 vs 54,05) e hipoglicemia noturna confirmada (6,03 vs 7,60) foram comparáveis com Insulina Degludeca versus a insulina detemir. Em ambos os braços de tratamento, crianças com idade entre 6-11 anos tiveram uma taxa numericamente mais elevada de hipoglicemia confirmada que nos outros grupos etários. Foi observada uma taxa elevada de hipoglicemia grave em crianças de 6 a 11 anos no braço Insulina Degludeca. A taxa de episódios hiperglicémicos com cetose foi significativamente menor para Insulina Degludeca versus a insulina detemir, 0,68 e 1,09, respectivamente. A frequência, tipo e gravidade das reações adversas na população pediátrica não indicam diferenças com a experiência da população geral de diabetes.
Desenvolvimento de anticorpos foi esparso e não tiveram impacto clínico. Dados de eficácia e segurança para pacientes adolescentes com diabetes mellitus tipo 2 foram extrapolados a partir de dados de pacientes adolescentes e adultos com diabetes mellitus tipo 1 e pacientes adultos com diabetes mellitus tipo 2. Os resultados suportam o uso de Insulina Degludeca em pacientes adolescentes com diabetes mellitus tipo 2.
Tabela 2. Diabetes Mellitus tipo 1 6, 7 :

Tabela 3 Diabetes Mellitus tipo 2 2, 3 :
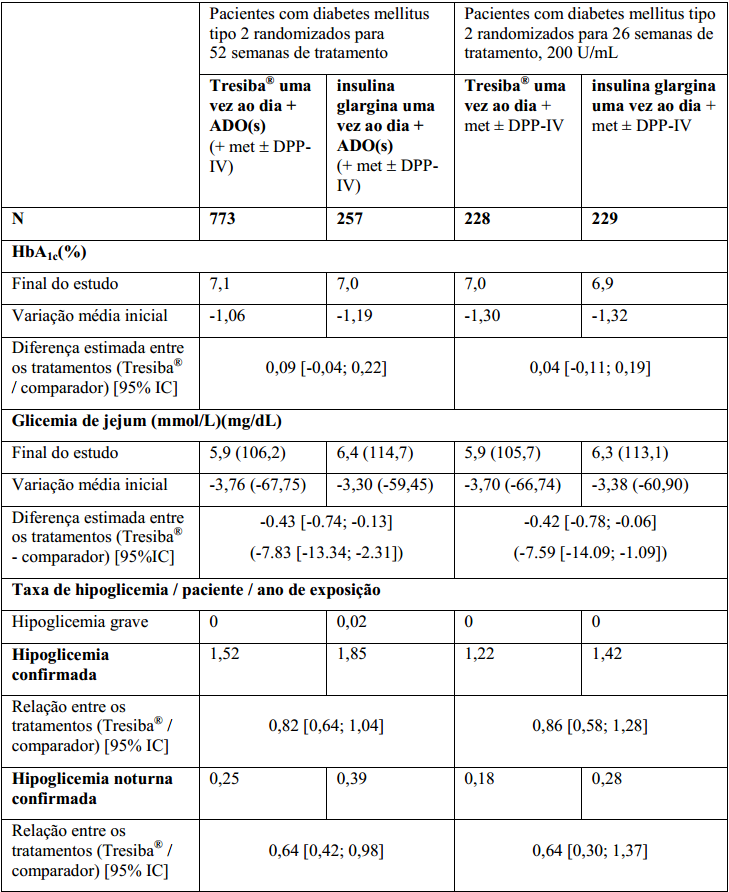
Tabela 4. Diabetes Mellitus tipo 2 1, 5 :
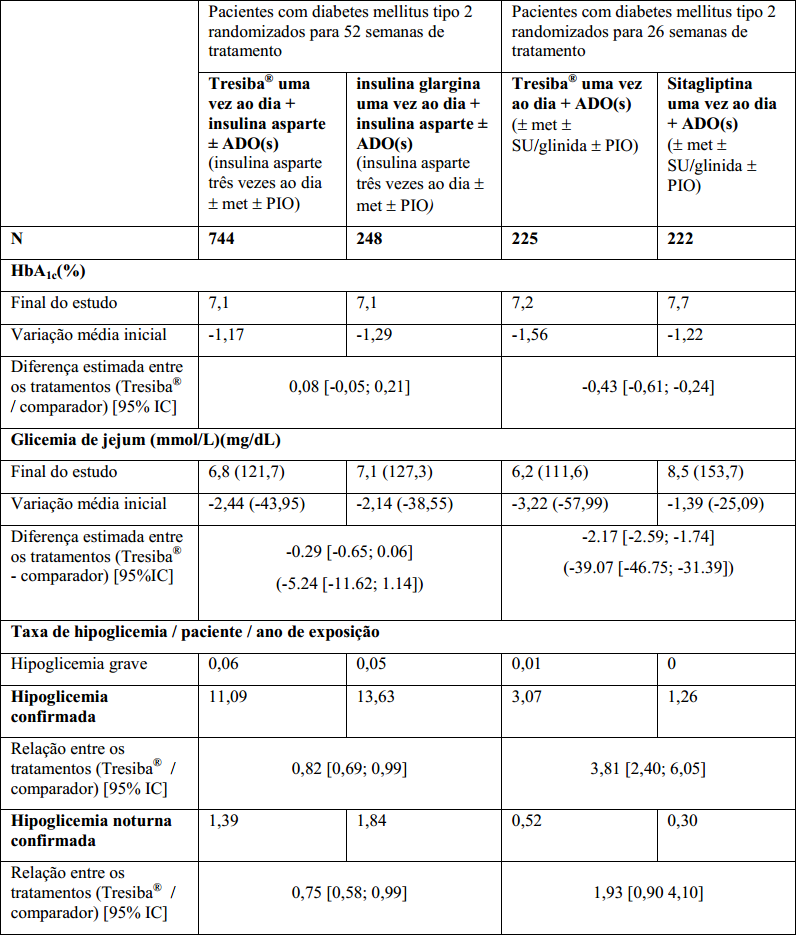
Pacientes adultos com diabetes mellitus tipo 2 randomizados para 26 semanas de tratamento com Insulina Degludeca, em dose única diária (com a refeição principal da noite) ou em esquema de dose flexível (intervalos entre as doses de 8 ou 40 horas aproximadamente) ou insulina glargina uma vez ao dia como parte da terapia combinada com um ou dois dos seguintes antidiabéticos orais (SU, metformina ou pioglitazona).
Tabela 5. Diabetes Mellitus tipo 2 uma vez ao dia ou esquema flexível 4 :

Referências:
1. Garber Alan J, King Allen B, Del Prato Stefano, Sreenan Seamus, Balci Mustafa K, Muñoz-Torres Manuel, Rosenstock Julio, Endahl Lars A, Francisco Ann Marie Ocampo, Hollander Priscilla. Insulin degludec, an ultra-longacting basal insulin, versus insulin glargine in basal-bolus treatment with mealtime insulin aspart in type 2 diabetes (BEGIN Basal-Bolus Type 2): a phase 3, randomised, open-label, treat to-target non-inferiority trial. Lancet 2012; 379 (9825): 1498-507.
2. The BEGIN™ Once Long Trial: Insulin degludec, an ultra-long-acting basal insulin, compared with insulin glargine in insulinnaïve patients with type 2 diabetes in a 1-year, phase 3, randomised, parallel-group, multinational, treat-to-target trial. Diabetes Care 2012; 35 (12): 2464-2471.
3. Gough Stephen C L, Bhargava Anuj, Jain Rajeev, Mersebach Henriette, Rasmussen Søren, Bergenstal Richard M. Low-Volume Insulin Degludec 200 units/mL Once Daily Improves Glycemic Control Similar to Insulin Glargine With a Low Risk of Hypoglycemia in Insulin-Naive Patients With Type 2 Diabetes: A 26 week, randomized, controlled, multinational, treat-to-ta.rget trial: The BEGIN LOW VOLUME trial. Diabetes care; 36 (9): 2536-2542.
4. Meneghini Luigi, Atkin Stephen L, Gough Stephen C L, Raz Itamar, Blonde Lawrence, Shestakova Marina, Bain Stephen, Johansen Thue, Begtrup Kamilla, Birkeland Kåre I. The Efficacy and Safety of Insulin Degludec Given in Variable Once-Daily Dosing Intervals Compared With Insulin Glargine and Insulin Degludec Dosed at the Same Time Daily: A 26-week, randomized,open-label, parallel-group, treat-to-target trial in people with type 2 diabetes. Diabetes care 2013; 36 (4): 858-864.
5. Philis-Tsimikas A, Del Prato S, Satman I, Bhargava A, Dharmalingam M, Skjøth T V, Rasmussen S, Garber A J. Effect of insulin degludec versus sitagliptin in patients with type 2 diabetes uncontrolled on oral antidiabetic agents. Diabetes, Obesity and Metabolism; 15 (8): 760–766.
6. Bode B, Buse J, Fisher M, Garg S, Marre M, Merker L, Renard E, Russell-Jones D, CTMH, AZRN, Heller S. Insulin Degludec Improves Glycemic Control with Lower Nocturnal Hypoglycemia Risk than Insulin Glargine in Basal-Bolus Treatment with Mealtime Insulin Aspart in Type 1 Diabetes (BEGIN Basal-Bolus Type 1): 2-year Results. Diabetic Medicine 2013; 30 (11) 1293-7.
7. Davies M J, Gross J L, Ono Y, Sasaki T, Bantwal G, Gall M A, Niemeyer M, Seino H. Efficacy and safety of insulin degludec given as part of basal-bolus treatment with mealtime insulin aspart in type 1 diabetes: a 26-week randomised, open-label, treat totarget non-inferiority trial. Diabetes, Obesity and Metabolism 2014. 16(10):922-930.
8. Mathieu Chantal, Hollander Priscilla, Miranda-Palma Bresta, Cooper John, Franek Edward, Russell-Jones David, Larsen Jens, Tamer Søren Can, Bain Stephen C. Efficacy and safety of insulin degludec in a flexible dosing regimen vs insulin glargine in patients with type 1 diabetes (BEGIN: Flex T1): a 26-week randomized, treat-to-target trial with a 26-week extension.The Journal of clinical endocrinology and metabolism 2013; 98 (3): 1154-62.
9. Ratner R E, Gough S C L, Mathieu C, Del Prato S, Bode B, Mersebach H, Endahl L, Zinman B. Hypoglycaemia risk with insulin degludec compared with insulin glargine in type 2 and type 1 diabetes: a pre-planned meta-analysis of phase 3 trials. Diabetes, Obesity and Metabolism 2012; 15 (2): 175-84.
10. Thlanage N. et al - Insulin degludec in combination with bolus insulin aspart is safe and effective in children and adolescents with type 1 diabetes. Pediatric Diabetes 2015. 16(3): 164-176.
11. Mathieu C, Rodbard H W, Cariou B, Handelsman Y, Philis-Tsimikas A, Ocampo Francisco A M, Rana A, Zinman B. A comparison of adding liraglutide versus a single daily dose of insulin aspart to insulin degludec in subjects with type 2 diabetes (BEGIN: VICTOZA ADD-ON). Diabetes, Obesity and Metabolism 2014; 16 (7): 636-44.
Características Farmacológicas
Propriedades farmacodinâmicas
Mecanismo de ação
A Insulina Degludeca liga-se especificamente ao receptor de insulina humana resultando nos mesmos efeitos farmacológicos da insulina humana.
O efeito de diminuição da glicemia pela Insulina Degludeca é causado pela absorção facilitada da glicose após a ligação da insulina aos receptores nos músculos e nas células adiposas e pela inibição simultânea da liberação de glicose pelo fígado.
Efeitos farmacodinâmicos
Insulina Degludeca é uma insulina basal de ação ultralonga que forma multi-hexâmeros solúveis após a aplicação subcutânea, resultando em um depósito do qual a Insulina Degludeca é contínua e lentamente absorvida na circulação levando a um efeito hipoglicemiante linear e estável. Durante um período de 24 horas com uma dose diária de tratamento, o efeito hipoglicemiante de Insulina Degludeca, em contraste com as atuais insulinas basais, foi uniformemente distribuído entre o primeiro e o segundo período de 12 horas (AUC GIR,0-12h,Estado de Equilíbrio / AUC GIR,total,Estado de Equilíbrio = 0,5 ).
Figura 3. Perfil médio de infusão de glicose com Insulina Degludeca (em estado de equilíbrio) em portadores de diabetes mellitus tipo 2.:
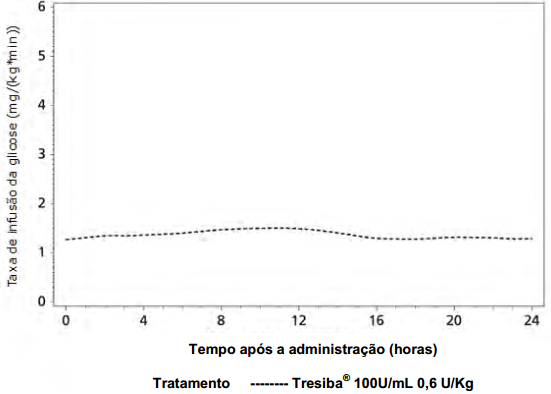
A duração da ação de Insulina Degludeca é maior do que 42 horas dentro da faixa de dose terapêutica.
Em um estudo de clamp euglicêmico com duração de 42 horas, realizado no estado de equilíbrio, os indivíduos que haviam recebido Insulina Degludeca 0,6 U/kg (n = 21) não apresentaram elevações da glicemia durante o período do estudo. Portanto, nestes indivíduos, a duração da ação foi superior a 42 horas.
O estado de equilíbrio é alcançado após 2-3 dias das administrações das doses. A ação de redução de glicemia da Insulina Degludeca no estado de equilíbrio mostrou variabilidade diária quatro vezes menor em termos de coeficientes de variação (CV) para o efeito hipoglicemiante durante um intervalo de dose (AUC GIR,τ, Estado de Equilíbrio ) e 2-24 horas (AUCGIR2-24h, Estado de Equilíbrio), em comparação com a insulina glargina.
Tabela 6. Variabilidade diária do efeito hipoglicemiante de Insulina Degludeca e insulina glargina no estado de equilíbrio em portadores de diabetes mellitus tipo 1:
| - | Insulina Degludeca (N=26) (CV%) | Insulina glargina (N=27) (CV%) |
| Variabilidade diária do efeito hipoglicemiante durante um intervalo de dose (AUC GIR,τ, Estado de Equilíbrio ) | 20 | 82 |
| Variabilidade diária do efeito hipoglicemiante de 2 a 24 horas (AUC GIR2-24h, Estado de Equilíbrio ) | 22 | 92 |
CV: coeficiente de variação intra-indivíduo em %.
AUC GIR,2-24h : efeito metabólico nas últimas 22 horas após a administração da dose (ou seja, não influenciado pela insulina intravenosa durante o período do clamp glicêmico).
O efeito hipoglicemiante total da Insulina Degludeca aumenta linearmente com o aumento da dose.
O efeito hipoglicemiante total é comparável para Insulina Degludeca 100 U/mL e 200 U/mL, quando administrados na mesma dose total.
Não há diferença clinicamente relevante na farmacodinâmica de Insulina Degludeca entre indivíduos adultos jovens e idosos.
Propriedades farmacocinéticas
Absorção
A ação ultralonga da Insulina Degludeca deriva da sua estrutura molecular especialmente projetada. Após a administração subcutânea, multi-hexâmeros solúveis e estáveis são formados criando um depósito de insulina no tecido subcutâneo. Os monômeros de Insulina Degludeca gradualmente separam-se dos multi-hexâmeros resultando em uma liberação lenta e contínua de Insulina Degludeca na circulação. Além disso, durante um período de 24 horas com uma dose diária de tratamento, a exposição da Insulina Degludeca foi uniformemente distribuída entre o primeiro e o segundo período de 12 horas (AUC Insulina Degludeca,0-12h,estado de equilíbrio / AUC Insulina Degludeca,Total,estado de equilíbrio = 0,5 ).
As concentrações séricas no estado de equilíbrio são alcançadas após 2-3 dias das administrações das doses.
Distribuição
A afinidade da Insulina Degludeca com a albumina sérica resulta em uma ligação às proteínas plasmáticas > 99% no plasma humano.
Metabolismo
A degradação da Insulina Degludeca é similar à da insulina humana; todos os metabólitos formados são inativos.
Eliminação
A meia-vida após a administração subcutânea é determinada pela taxa de absorção do tecido subcutâneo. A meia-vida da Insulina Degludeca é de aproximadamente 25 horas independente da dose.
Linearidade
A proporcionalidade da dose na exposição total é observada após a administração subcutânea dentro da faixa de dose terapêutica. Na comparação direta, requisitos para a bioequivalência são cumpridos para Insulina Degludeca 100 U/mL e Insulina Degludeca 200 U/mL (com base na AUC Insulina Degludeca,τ, Estado de Equilíbrio e C max, Insulina Degludeca, Estado de Equilíbrio ).
Gênero
Não há diferença entre os gêneros nas propriedades farmacocinéticas de Insulina Degludeca.
Idosos, raça. insuficiência renal ou hepática
Não há diferença na farmacocinética da Insulina Degludeca entre pacientes idosos, adultos e jovens, entre raças, ou entre pacientes saudáveis e indivíduos com insuficiência renal ou hepática.
Crianças e adolescentes
As propriedades farmacocinéticas da Insulina Degludeca em crianças (1-11 anos) e adolescentes (12-18 anos) foram comparáveis no estado de equilíbrio àquelas observados em adultos com diabetes mellitus tipo 1. A exposição total após uma única dose fixa foi maior em crianças/adolescentes do que em adultos com diabetes mellitus tipo 1.
Dados de segurança pré-clínicos
Os dados pré-clínicos não revelaram preocupações de segurança para os humanos com base em estudos de segurança farmacológica, toxicidade de dose repetida, potencial carcinogênico e toxicidade reprodutiva.
A taxa de mitogênese relativa à potência metabólica para Insulina Degludeca mantém-se inalterada em comparação com a insulina humana.
Como devo armazenar o Tresiba?
Antes do uso
Conservar sob refrigeração (entre 2 °C e 8 °C). Mantenha o medicamento distante do compartimento do congelador. Não congelar.
Em uso ou carregados como reserva
Tresiba ® FlexTouch ® 100 U/mL
- Você pode levar Tresiba ® FlexTouch ® com você e mantê-lo à temperatura ambiente (abaixo de 30 °C) ou sob refrigeração (entre 2 °C e 8 °C), por até 8 semanas.
- Após aberto, Tresiba ® deve ser mantido em temperatura ambiente, (inferior a 30 °C) ou sob refrigeração (entre 2 °C e 8 °C), longe do calor direto e tampado para proteger da luz, por no máximo 8 semanas (56 dias).
- Sempre mantenha o sistema de aplicação tampado quando você não estiver usando, para proteger da luz. Tresiba ® deve ser protegido do calor e luz excessivos.
Tresiba ® Penfill ® 100 U/mL
- Não refrigerar. Você pode levar Tresiba ® Penfill ® com você e mantê-lo à temperatura ambiente (abaixo de 30 °C) por até 8 semanas.
- Sempre mantenha o sistema de aplicação tampado quando você não estiver usando, para proteger da luz. Tresiba ® deve ser protegido do calor e luz excessivos.
- Após aberto, Tresiba ® deve ser mantido em temperatura ambiente, inferior a 30 °C, longe do calor direto e tampado para proteger da luz, por no máximo 8 semanas (56 dias). Tresiba ® deve ser descartado 56 dias após ter sido inicialmente retirado da refrigeração, mesmo que ainda tenha produto no carpule.
- Sempre mantenha Tresiba ® dentro da embalagem quando você não estiver usando, para proteger da luz. Tresiba ® deve ser protegido do calor e luz excessivos.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Número de lote e datas de fabricação e validade: Vide embalagem.
O prazo de validade corresponde ao último dia do mês indicado.
Transporte
O transporte do medicamento deverá ser realizado através de uma embalagem que proporcione proteção térmica e evite alteração brusca de temperatura, incidência de luz direta e vibração excessiva. No caso de viagens aéreas, não despachar o produto dentro das malas. O compartimento de bagagem dos aviões atinge temperaturas muito baixas, podendo congelar o medicamento.
Descarte
O descarte de agulhas deve ser realizado através de embalagens coletoras resistentes, como latas e plásticos, para eliminar o risco de acidentes e contaminação. Os medicamentos usados, vencidos ou fora de uso, assim como seu sistema de aplicação e as embalagens coletoras contendo as agulhas, devem ser descartados em Postos de Coleta localizados em Farmácias, Drogarias, Postos de Saúde ou Hospitais, que possuem coletores apropriados. O cartucho e a bula que não possuem contato direto com o medicamento, podem ser descartados no lixo reciclável.
Em caso de dúvidas consulte seu farmacêutico, enfermeiro, médico ou vigilância sanitária.
Exclusivo Tresiba ® FlexTouch ® 100 U/mL: Não tente repor o conteúdo do sistema de aplicação ou reutilizá-lo. Uma vez vazio, ele deve ser descartado.
Características do medicamento
Tresiba ® é uma solução límpida e incolor.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais do Tresiba
M.S - 1.1766.0029
Farmacêutico responsável:
Luciane M. H. Fernandes
CRF/PR n° 6002
Fabricado por:
Novo Nordisk A/S
Bagsværd, Dinamarca
Ou
Novo Nordisk Production SAS
Chartres, França (vide cartucho)
Registrado por:
Novo Nordisk Farmacêutica do Brasil Ltda
Rua Prof. Francisco Ribeiro, 683
Araucária/PR
CNPJ: 82.277.955/0001-55
Importado por:
Novo Nordisk Farmacêutica do Brasil Ltda
Rua Francisco Munõz Madrid, 625
São José dos Pinhais/PR
SAC
0800 144488
Tresiba ® e FlexTouch ® são marcas registradas de propriedade da Novo Nordisk A/S, Dinamarca
© 2020
Novo Nordisk A/S
Tresiba ® e Penfill ® são marcas registradas de propriedade da Novo Nordisk A/S
© 2020
Novo Nordisk A/S
Venda sob prescrição médica.
















