Levemir
Bula do Medicamento - Farmacologia do Remédio
Levemir, para o que é indicado e para o que serve?
Levemir ® é indicado para o tratamento de diabetes mellitus em adultos, adolescentes e crianças acima de 1 ano de idade.
Como o Levemir funciona?
Diabetes mellitus é uma doença na qual seu organismo não produz insulina suficiente para controlar o nível de açúcar no sangue.
Levemir ® diminui a concentração de açúcar no sangue (glicemia).
Levemir ® é uma insulina moderna (insulina análoga) de longa duração (até 24 horas). Insulinas modernas são versões aperfeiçoadas da insulina humana. Comparado com outras insulinas, o tratamento com Levemir ® está associado com menor ganho de peso.
Quais as contraindicações do Levemir?
Você não deve usar Levemir ® :
- Se você for alérgico (hipersensível) a insulina detemir ou qualquer um dos componentes da fórmula de Levemir ® ;
- Se você sentir sintomas de hipoglicemia (baixo nível de açúcar no sangue);
- Em bombas de infusão de insulina;
- Se Levemir foi derrubado, danificado ou amassado;
- Se não foi armazenado corretamente ou se foi congelado;
- Se a insulina não estiver límpida e incolor.
Este medicamento é contraindicado para menores de 1 ano.
Como usar o Levemir?
Levemir FlexPen / Levemir Penfill
Converse com seu médico sobre sua necessidade de insulina. Não altere sua insulina a menos que seu médico recomende. Assegure-se que você adquiriu Levemir ® , identificada pela cor, como seu médico lhe prescreveu e siga suas orientações cuidadosamente.
Se o seu médico trocou seu tipo ou sua marca de insulina para outra, sua dosagem deve ser ajustada por ele.
Antes de usar Levemir ®
- Verifique o rótulo para ter certeza de que este é o tipo correto de insulina;
- Sempre use uma agulha nova para cada injeção para prevenir contaminação;
- As agulhas e Levemir ® não devem ser compartilhados.
Exclusivo Levemir Penfill: Sempre verifique o carpule, incluindo o êmbolo de borracha. Não o utilize se estiver danificado ou se existir um espaço entre o êmbolo de borracha e a faixa branca do rótulo e devolva-o ao seu fornecedor. Veja o manual de instruções do sistema de aplicação para mais informações.
Exclusivo Levemir FlexPen: Veja as instruções de uso de Levemir ® ao final desta bula.
Método de aplicação
Levemir ® deve ser aplicado sob a pele (via subcutânea). Nunca injete insulina diretamente em uma veia (via intravenosa) ou músculo (via intramuscular). Levemir ® também pode ser utilizado em combinação com antidiabéticos orais ou com insulinas de ação rápida ou ultrarrápida administradas com as refeições. A cada aplicação, varie o local de injeção dentro da região específica da pele que você utiliza. Isto diminui o risco de formação de caroços ou lesões na pele.
Os melhores locais para aplicação são:
A parte da frente das suas coxas, os glúteos, a parte da frente da sua cintura (abdome) ou a parte superior do seu braço. A injeção pode ser aplicada a qualquer hora do dia, mas no mesmo horário todos os dias. Você deve medir sua glicose sanguínea regularmente.
Dosagem
Levemir ® também pode ser utilizado em combinação com antidiabéticos orais e/ou com agonistas do receptor de GLP-1 para o tratamento do diabetes mellitus tipo 2 em adultos.
Em combinação com antidiabéticos orais ou quando adicionado à terapia com agonistas do receptor de GLP-1, recomenda-se iniciar o tratamento com Levemir ® com a administração de uma dose de 0,1-0,2 U/kg ou 10U em pacientes adultos uma vez ao dia. Ao adicionar um agonista do receptor de GLP-1 ao tratamento com Levemir ® , é recomendado que a dose de Levemir ® seja reduzida em 20% para minimizar os riscos de hipoglicemia. A dosagem de Levemir ® deve ser ajustada individualmente.
Quando Levemir ® é utilizado como parte de um regime basal-bolus de insulina, Levemir ® deve ser administrado uma ou duas vezes ao dia, dependendo das necessidades do paciente. Para pacientes que requerem duas doses diárias, para otimizar o controle de glicose sanguínea, a dose da noite pode ser aplicada ao anoitecer, ou antes de dormir . O ajuste de dose pode ser necessário se o paciente apresentar aumento em suas atividades físicas, mudar sua dieta habitual ou se apresentar doenças concomitantes.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
Exclusivo Levemir FlexPen
Instruções de uso de Levemir ® FlexPen ®
Leia cuidadosamente as instruções a seguir antes de utilizar Levemir ® FlexPen ® .
Se você não seguir cuidadosamente as instruções de uso, você poderá injetar uma dose muito alta ou muito baixa de insulina, o que pode levar a um aumento ou uma diminuição excessiva do nível de açúcar no sangue.
Levemir ® FlexPen ® é um sistema de aplicação de insulina. Doses de 1 a 60 unidades em incrementos de 1 unidade podem ser selecionadas. Levemir ® FlexPen ® pode ser administrado com agulhas de até 8 mm de comprimento. Seu sistema de aplicação foi desenvolvido para ser utilizado com agulhas descartáveis NovoFine ® . Como medida de prevenção, sempre carregue um sistema de aplicação de insulina reserva no caso de perder ou danificar seu Levemir ® FlexPen ® .

Cuidando de seu FlexPen ®
Seu FlexPen ® deve ser manuseado com cuidado.
Se ele for derrubado, danificado ou quebrado, há riscos de vazamento de insulina. Isso pode causar imprecisão na dose, o que pode levar ao aumento ou à diminuição do nível de açúcar no sangue.
Você pode limpar a parte externa de seu FlexPen ® utilizando algodão umedecido em álcool. Não o deixe de molho, nem lave ou lubrifique, pois pode danificar o sistema de aplicação.
Não preencha seu FlexPen ® novamente.
Preparando Levemir ® FlexPen ®
Verifique o rótulo para ter certeza que Levemir ® FlexPen ® contém o tipo correto de insulina.
Isso é especialmente importante se você utiliza mais de um tipo de insulina. Se você selecionar e injetar o tipo errado, seu nível de açúcar no sangue pode aumentar ou diminuir muito.
- Retire a tampa do sistema de aplicação.
- Remova o selo protetor de uma agulha descartável nova. Rosqueie a agulha firmemente no Levemir ® FlexPen ® .
- Retire a tampa externa da agulha e guarde-a para depois.
- Retire a tampa interna da agulha e descarte-a. Nunca tente colocar de volta a tampa interna. Você pode se perfurar com a agulha.
- Use sempre uma agulha nova para cada aplicação. Isso reduz o risco de contaminação, infecção, vazamento de insulina, entupimento de agulhas e imprecisão de dose.
- Cuidado para não entortar ou danificar a agulha antes do uso.
Verificando o fluxo de insulina
Antes de cada injeção, pequenas quantidades de ar podem se acumular no carpule durante seu uso normal.
Para evitar a injeção de ar e ter certeza da dosagem adequada:
- Gire o seletor de dose para selecionar 2 unidades.
- Segure Levemir ® FlexPen ® com a agulha apontada para cima e bata levemente com o dedo no carpule algumas vezes para fazer com que qualquer bolha de ar vá para o topo do carpule.
- Mantendo a agulha para cima, pressione o botão injetor completamente. O seletor de dose retorna a 0 (zero).
Uma gota de insulina deve aparecer na ponta da agulha. Se não, troque a agulha e repita o procedimento não mais do que 6 vezes.
Se uma gota de insulina ainda não aparecer, o sistema de aplicação está com defeito e você deve utilizar um sistema de aplicação novo.
- Certifique-se sempre de que a gota apareça na ponta da agulha antes de injetar. Isso garante o fluxo de insulina. Se nenhuma gota aparecer, a insulina não será aplicada, mesmo que o contador de dose possa mover-se. Isso pode indicar agulha entupida ou danificada.
- Verifique sempre o fluxo de insulina antes de injetar. Se o fluxo não for verificado, uma dose muito baixa ou nenhuma dose de insulina pode ser injetada, Isso pode levar ao aumento do nível de açúcar no sangue.
Selecionando a dose
Verifique se o seletor de dose está ajustado a 0 (zero).
- Gire o seletor de dose para selecionar o número de unidades que você necessita injetar.
A dose pode ser corrigida para mais ou para menos, girando o seletor de dose em qualquer direção até que a dose correta esteja alinhada ao indicador. Ao girar o seletor de dose, tenha cuidado para não pressionar o botão injetor, pois a insulina poderá sair.
Você não pode selecionar uma dose maior do que o número de unidades disponíveis no carpule.
- Use sempre o contador de dose e o indicador de dose para ver quantas unidades você selecionou antes de injetar a insulina.
- Não conte pelos cliques do sistema de aplicação. Se você selecionar e injetar a dose errada, seu nível deaçúcar no sangue pode aumentar ou diminuir muito. Não use a escala residual, ela mostra apenas a quantidade de insulina que resta na sua caneta.
Injetando a insulina
Insira a agulha na sua pele. Utilize a técnica de injeção indicada pelo seu médico ou enfermeiro.
- Injete a dose pressionando o botão injetor completamente, até que o 0 (zero) se alinhe ao indicador. Certifique-se de apertar o botão injetor somente quando estiver efetuando a injeção.
Girar o seletor de dose não injetará insulina.
- Mantenha o botão injetor totalmente pressionado e mantenha a agulha sob a pele por pelo menos 6 segundos.
Isso garantirá que a dose total foi aplicada.
Retire a agulha da pele e em seguida, solte o botão injetor.
Certifique-se de que o seletor de dose retornou a 0 (zero) após a injeção. Se o seletor de dose parar antes de retornar a 0 (zero), a dose não terá sido aplicada por inteiro, o que pode resultar no aumento de açúcar no sangue.
- Leve a agulha para dentro da tampa externa sem tocar na tampa.
Quando a agulha estiver tampada, cuidadosamente pressione a tampa externa completamente e desrosque a agulha.
Descarte-a cuidadosamente e coloque a tampa da caneta no sistema de aplicação.
- Sempre remova a agulha após cada injeção e guarde seu Levemir ® FlexPen ® sem a agulha rosqueada. Isso reduz o risco de contaminação, infecção, vazamento de insulina, entupimento da agulha e imprecisão de dose.
Informações adicionais
- Cuidadores devem ser cautelosos para manusear agulhas usadas para evitar perfurações e infecção cruzada.
- Descarte seu Levemir ® FlexPen ® usado cuidadosamente sem a agulha rosqueada.
- As agulhas não devem ser compartilhadas. Isso pode levar a infecção cruzada.
- Levemir ® FlexPen ® não deve ser compartilhado. Sua medicação pode ser prejudicial à saúde de outras pessoas.
- Mantenha sempre seu dispositivo e agulhas fora do alcance de outras pessoas, especialmente crianças.
Exclusivo Levemir Penfill
Como injetar esta insulina
- Injete a insulina sob sua pele. Use a técnica de injeção recomendada pelo seu médico e descrita no manual de seu sistema de aplicação;
- Mantenha a agulha sob a pele por pelo menos 6 segundos. Mantenha o botão injetor totalmente pressionado até que a agulha tenha sido retirada da pele. Isto garante a injeção correta e diminui a possibilidade de entrada de sangue na agulha ou no carpule;
- Após cada injeção, assegure-se de remover e descartar a agulha. Armazene seu Levemir ® sem a agulha rosqueada. Caso contrário, o líquido pode vazar, o que pode causar dosagem incorreta.
Não preencha o carpule novamente.
Levemir ® foi desenvolvido para ser utilizado com sistemas de aplicação de insulina da Novo Nordisk e agulhas descartáveis NovoFine ® .
Se você é tratado com Levemir ® e outro carpule Penfill ® de insulina, você deve usar dois sistemas de aplicação de insulina, um para cada tipo de insulina.
Por precaução, tenha sempre um sistema de aplicação reserva, caso seu Levemir ® seja perdido ou danificado.
O que eu devo fazer quando esquecer de usar o Levemir?
Se você se esquecer de usar a sua insulina seu nível de açúcar no sangue pode ficar muito alto (isto é chamado hiperglicemia). Isto também pode acontecer:
- Se você injetar repetidamente menos insulina do que necessita;
- Se você tiver uma infecção ou febre;
- Se você comer mais do que o habitual;
- Se você fizer menos exercícios do que o habitual.
Os sinais de alerta aparecem gradualmente. Eles incluem:
Aumento do volume de urina, sede, perda de apetite, náusea ou vômito , sonolência ou cansaço, pele seca com vermelhidão, boca seca e hálito com cheiro de fruta (cetona). Esses podem ser sinais de uma condição muito séria chamada cetoacidose diabética (acúmulo de ácido no sangue, pois o organismo está utilizando gordura ao invés de açúcar). Se você não tratá-la, esta condição pode resultar em coma diabético e eventualmente morte.
Se você apresentar qualquer um desses sinais, teste seu nível de açúcar no sangue, teste sua urina para cetonas, se possível, e procure orientação médica imediatamente.
Se você parar de usar sua insulina:
Isto pode levar a hiperglicemia grave (nível muito alto de açúcar no sangue) e cetoacidose. Não pare de usar sua insulina sem consultar seu médico, ele lhe dirá o que é necessário ser feito.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Quais cuidados devo ter ao usar o Levemir?
Leia toda a bula com atenção antes de começar a usar sua insulina.
Mantenha esta bula com você. Você pode precisar lê-la novamente.
Se você tiver dúvidas adicionais, pergunte ao seu médico, enfermeiro ou farmacêutico.
Este medicamento foi prescrito para você. Não o dê para outras pessoas, pois poderá causar danos até mesmo se os sintomas forem os mesmos que os seus.
Se qualquer efeito colateral piorar, ou se você notar qualquer efeito colateral não mencionado nesta bula, consulte seu médico, enfermeiro ou farmacêutico.
Tenha cuidado especial com Levemir ® :
- Se você tiver problemas nos rins ou fígado , ou nas glândulas suprarrenais, hipófise ou tireoide ;
- Se você se exercitar mais que o habitual, ou se você quiser alterar sua dieta, já que isso pode afetar seu nível de açúcar no sangue;
- Se você estiver doente continue usando sua insulina e consulte seu médico;
- Se você for viajar a longa distância: viajar para regiões com fuso horário diferente pode alterar sua necessidade de insulina e o intervalo de suas aplicações. Consulte seu médico, se você está planejando viajar.
Levemir ® não deve ser diluída ou misturada com nenhuma outra preparação de insulina.
Alterações da pele no local da injeção
O local da injeção deve ser alternado para ajudar a prevenir alterações no tecido adiposo sob a pele, tais como espessamento da pele, encolhimento da pele ou caroços sob a pele. A insulina pode não funcionar muito bem se você injetar em uma área irregular, encolhida ou mais espessa. Informe o seu médico se você detectar quaisquer alterações da pele no local da injeção.
Informe o seu médico se atualmente você estiver injetando nessas áreas afetadas antes de começar a injetar em uma área diferente. O seu médico pode pedir-lhe para verificar mais frequentemente o nível de açúcar no sangue e ajustar a dose de insulina ou de outros medicamentos antidiabéticos.
Uso em crianças
Levemir ® pode ser usado em adolescentes e crianças acima de 1 ano de idade.
Não existem dados com relação ao uso de Levemir ® em crianças abaixo de 1 ano de idade.
Dirigindo e usando máquinas
Se seu nível de açúcar no sangue estiver baixo ou alto, sua concentração ou habilidade de reagir poderá ser afetada como também sua habilidade de dirigir ou operar uma máquina.
Considere que você poderá colocar outras pessoas em perigo ou a si mesmo. Converse com seu médico se você pode dirigir:
- Se você apresenta hipoglicemia frequentemente;
- Se você tem dificuldade em reconhecer uma hipoglicemia.
Este medicamento pode causar doping .
Quais as reações adversas e os efeitos colaterais do Levemir?
Assim como qualquer medicamento, Levemir ® pode causar efeitos colaterais, embora nem todas as pessoas os apresentem.
Os efeitos colaterais podem aparecer em certas frequências, como a seguir:
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento)
Baixo nível de açúcar no sangue (hipoglicemia). Vide advertência em “ Superdose: o que acontece se tomar uma dose do Levemir maior do que a recomendada? ”.
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento)
Reações no local da injeção (dor, vermelhidão, urticária , inflamação, hematoma, inchaço e coceira). Elas geralmente desaparecem após algumas semanas de tratamento com insulina. Se não desaparecerem, procure seu médico. Se você apresentar reações sérias ou frequentes, você pode precisar parar o tratamento com Levemir ® e usar outra insulina.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento)
Sinais de alergia: urticária e erupção cutânea (reação de pele) podem ocorrer.
Procure orientação médica imediatamente
- Se os sinais de alergia acima aparecerem ou;
- Se você repentinamente sentir-se indisposto, e começar a suar, vomitar, ter dificuldade para respirar, ter palpitações, apresentar tonturas.
Distúrbios visuais
No início do tratamento com insulina, pode ocorrer distúrbio de sua visão, mas é um distúrbio geralmente temporário.
- Alterações da pele no local da injeção: Se você injetar insulina no mesmo local, o tecido adiposo pode encolher (lipoatrofia) ou ficar mais espesso (lipohipertrofia) (podem ocorrer em até 1 em 100 pessoas). Caroços sob a pele também podem ser causados pelo acúmulo de uma proteína chamada amilóide ( amiloidose cutânea, a frequência com que isso ocorre é desconhecida). A insulina pode não funcionar muito bem se você injetar em uma área irregular, encolhida ou mais espessa. Alterne o local da injeção a cada aplicação para ajudar a prevenir essas alterações na pele.
- Inchaço nas articulações: quando você iniciar o uso de insulina, a retenção de água pode causar inchaço no tornozelo e outras articulações. Normalmente, isto desaparece em pouco tempo.
- Retinopatia diabética (uma doença dos olhos relacionada ao diabetes que pode levar a perda da visão). Se você tem retinopatia diabética e seu nível de açúcar no sangue melhorar muito rápido, a retinopatia pode piorar. Pergunte ao seu médico sobre isto.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento)
Neuropatia dolorosa (dor devido a lesão no nervo). Se o nível de açúcar no sangue melhorar muito rápido, você pode ter dor relacionada ao nervo, isto é chamado neuropatia dolorosa aguda e é, geralmente, passageira.
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento)
Reação alérgica grave a Levemir ® ou a um de seus componentes (chamada de reação alérgica sistêmica).
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
População Especial
Se você tem função reduzida dos rins ou fígado, ou se você tem mais de 65 anos, você deve verificar seu nível de açúcar no sangue com maior regularidade e discutir as alterações na sua dose de insulina com seu médico.
Gravidez e amamentação
Se você está grávida não pare de usar sua insulina e procure orientação médica ou do cirurgião-dentista.
Este medicamento pode ser utilizado durante a gravidez desde que sob prescrição médica ou do cirurgião-dentista.
Se você está grávida, planejando engravidar, ou amamentando procure seu médico para orientação quando estiver usando este medicamento, pois a dose de insulina pode necessitar de alteração durante a gravidez e após o parto. O controle cuidadoso e a prevenção de hipoglicemia são importantes para a saúde do seu bebê.
O risco de defeitos congênitos, a perda de gravidez ou outros eventos adversos que existem para todas as gestações, é aumentado em gestações complicadas pela hiperglicemia . Pacientes do sexo feminino devem ser aconselhadas a informar o seu médico se estão tentando engravidar ou se ficarem grávidas durante o tratamento com Levemir ® . Um estudo clínico randomizado e controlado de mulheres grávidas com diabetes tipo I, utilizando Levemir ® durante a gravidez, não demonstrou aumento no risco de anomalias fetais.
Estudos de toxicidade reprodutiva em coelhos e ratos não-diabéticos, que incluiu grupos de controle de insulina humana concorrentes, indicaram que a insulina detemir e a insulina humana tiveram efeitos similares em relação à embriotoxicidade (efeitos adversos tóxicos sobre o embrião devido a passagem através da barreira placentária da substância para dentro do sistema materno) e teratogenicidade (propriedade ou capacidade de gerar malformações congênitas), que foram atribuídos à hipoglicemia materna.
O tratamento com Levemir ® pode ser considerado durante a gravidez, somente se os benefícios justificarem os possíveis riscos.
Se você estiver amamentando consulte seu médico, pois pode ser necessário o ajuste da dose de sua insulina.
Apresentações do Levemir
Levemir ® FlexPen ®
Solução injetável - insulina detemir 100 U/mL, em sistema de aplicação preenchido.
Embalagem contendo 1 ou 5 sistema(s) de aplicação preenchido(s) de Levemir ® FlexPen ® , com 3 mL cada.
Via subcutânea.
Uso adulto e pediátrico acima de 1 ano.
Levemir ® Penfill ®
Solução injetável - insulina detemir 100 U/mL, em carpule.
Embalagem contendo 1 ou 5 carpule(s) de Levemir ® Penfill ® com 3 mL.
Via subcutânea.
Uso adulto e pediátrico acima de 1 ano.
Qual a composição do Levemir?
Cada mL da solução injetável contém 100 U de insulina detemir (equivalente a 14,2 mg) produzida por tecnologia de DNA recombinante.
Excipientes: glicerol , fenol, metacresol, acetato de zinco , fosfato de sódio dibásico di-hidratado, cloreto de sódio , hidróxido de sódio, ácido clorídrico e água para injetáveis .
Cada sistema de aplicação preenchido de Levemir ® FlexPen ® e Levemir ® Penfill ® contém 3 mL de solução equivalente a 300 U.
Uma unidade (U) de insulina detemir corresponde a uma unidade internacional (UI) de insulina humana.
Superdose: o que acontece se tomar uma dose do Levemir maior do que a recomendada?
Se você aplicar uma grande quantidade de insulina, o nível de açúcar em seu sangue pode ficar muito baixo (isto é chamado de hipoglicemia). Isto também pode acontecer:
- Se você comer muito pouco ou pular uma refeição;
- Se você se exercitar mais do que o habitual.
Os sinais de alerta de uma hipoglicemia podem aparecer repentinamente e podem incluir:
Suor frio, pele fria e pálida, cefaleia ( dor de cabeça ), palpitação, mal estar, fome excessiva, alterações temporárias na visão, sonolência, fraqueza e cansaço incomuns, nervosismo ou tremor, sentimento de ansiedade , sensação de confusão e dificuldade de concentração.
Se você sentir alguns destes sinais de hipoglicemia, coma um alimento rico em açúcar e logo meça seu nível de açúcar no sangue. Se o seu nível de açúcar no sangue estiver muito baixo coma um pouco de açúcar ou um alimento rico em açúcar (doces, biscoitos, suco de fruta), depois descanse.
Sempre carregue consigo doces, biscoitos, suco de fruta, por precaução.
Quando os sintomas de hipoglicemia tiverem desaparecido ou quando os níveis de glicose no sangue estiverem estáveis, continue seu tratamento com insulina.
Informe seus parentes e amigos que você é portador de diabetes e quais podem ser as consequências, incluindo o risco de desmaio durante a hipoglicemia.
Informe seus parentes e amigos que se você desmaiar, eles devem virar você de lado e procurar ajuda médica imediatamente. Eles não devem dar a você qualquer comida ou bebida. Isso pode engasgá-lo.
Você pode se recuperar mais rapidamente da inconsciência com uma injeção do hormônio glucagon dado poralguém que saiba como injetá-lo. Se você receber glucagon, você precisará de glicose ou de um alimento doce assim que recuperar a consciência. Se você não responder ao tratamento com glucagon, você terá de ser tratado no hospital. Entre em contato com seu médico após uma injeção de glucagon para descobrir a razão da sua hipoglicemia a fim de evitá-la outras vezes.
- Se uma hipoglicemia grave prolongada não for tratada, ela poderá causar dano cerebral (temporário ou permanente) e até mesmo morte.
- Se você tiver uma hipoglicemia que fizer você desmaiar, ou hipoglicemias frequentes, converse com seu médico. A quantidade ou intervalo de aplicações de sua insulina, sua alimentação ou exercícios podem necessitar de ajustes.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação medicamentosa: quais os efeitos de tomar Levemir com outros remédios?
Alguns medicamentos afetam a forma como a glicose atua em seu corpo e isso pode influenciar na dose de insulina. Abaixo estão listados os medicamentos mais comuns que podem afetar seu tratamento com insulina.
Fale com seu médico, enfermeiro ou farmacêutico se você está tomando ou tomou recentemente qualquer outro medicamento, mesmo aqueles obtidos sem receita médica. Em particular, informe seu médico se você estiver usando algum dos medicamentos abaixo mencionados, os quais afetam seu nível de açúcar no sangue.
Se você usar algum dos medicamentos abaixo, seu nível de açúcar no sangue pode diminuir (hipoglicemia):
- Outros medicamentos para o tratamento do diabetes;
- Inibidores da monoaminoxidase (IMAO) (usados para tratar depressão );
- Beta-bloqueadores (usados para tratar pressão alta );
- Inibidores da enzima conversora da angiotensina (ECA) (usados para tratar certas condições cardíacas ou pressão alta);
- Salicilatos (usados para aliviar a dor e baixar a febre );
- Esteroides anabólicos (como testosterona );
- Sulfonamidas (usadas para tratar infecções).
Se você usar algum dos medicamentos abaixo, seu nível de açúcar no sangue pode aumentar (hiperglicemia):
- Anticoncepcionais orais (para o controle de natalidade);
- Tiazidas (usadas para tratar hipertensão arterial e retenção excessiva de líquido);
- Glicocorticoides (como “cortisona”, usados no tratamento da inflamação);
- Hormônios da tireoide (usados para tratar distúrbios da glândula tireoide);
- Simpatomiméticos (como epinefrina [adrenalina], ou salbutamol , terbutalina , usados para tratar asma );
- Hormônio de crescimento (medicamento para estimulação do crescimento somático e esquelético e que exerce grande influência nos processos metabólicos do corpo);
- Danazol (medicamento que atua na ovulação).
Octreotida e lanreotida (usados no tratamento de acromegalia , um distúrbio hormonal raro que, geralmente, ocorre em adultos de meia idade, causada pelo excesso de produção de hormônio de crescimento pela hipófise) podem aumentar ou diminuir seu nível de açúcar no sangue.
Beta-bloqueadores (usados para tratar pressão alta) podem diminuir ou eliminar inteiramente os primeiros sintomas de alerta que ajudam a reconhecer uma hipoglicemia.
Tiazolidinedionas (classe de medicamentos antidiabéticos orais usados para o tratamento de diabetes tipo 2). Alguns portadores de diabetes tipo 2 de longa data, doença cardíaca ou derrame prévio que são tratados com tiazolidinedionas em combinação com insulina podem desenvolver insuficiência cardíaca . Informe seu médico assim que possível se você apresentar sinais de insuficiência cardíaca, assim como falta de ar ou aumento rápido no peso ou inchaço localizado ( edema ).
Usando Levemir ® com alimentos e álcool
Se você ingerir álcool sua necessidade de insulina pode mudar, pois seu nível de açúcar no sangue pode aumentar ou diminuir. É recomendado um monitoramento cuidadoso.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Qual a ação da substância do Levemir (Insulina Detemir)?
Resultados de eficácia
O efeito redutor da glicose da Insulina Detemir é dose-dependente. O uso de Insulina Detemir vem sendo investigado em crianças a partir dos dois anos, em adolescentes e em adultos. A Insulina Detemir possui menor variabilidade entre pacientes do que a NPH e possui um efeito metabólico mais previsível, incluindo uma menor variabilidade diária em GPJ e um menor risco relativo de hipoglicemia noturna do que a NPH. Além disto, a Insulina Detemir oferece menor ganho de peso do que a NPH. A combinação de Insulina Detemir e insulina asparte em terapia basal- bolus oferece melhor controle glicêmico com menor risco de hipoglicemia, em comparação com a combinação de NPH e HSI.
Estudos em pacientes com diabetes tipo 2 tratados com insulina basal em associação com medicamentos antidiabéticos orais demonstraram que o controle glicêmico (HbA 1c ) com Insulina Detemir é comparável ao obtido com a insulina NPH e insulina glargina e está associado a menor ganho de peso. Veja Tabela 1.
Tabela 1. Alteração no peso corporal após tratamento com insulina

Em estudos com o uso da terapia de combinação-ADO, o tratamento com Insulina Detemir resultou em um risco 61-65% menor de hipoglicemia noturna em comparação com a insulina NPH.
Em estudos clínicos utilizando a terapia insulínica basal- bolus , as taxas globais de hipoglicemia com Insulina Detemir e insulina NPH foram similares. A análise de hipoglicemia noturna em pacientes com diabetes tipo 1 mostrou um risco significativamente reduzido de hipoglicemia noturna (capaz de auto tratamento e confirmado por glicemia capilar menor que 2,8 mmol/L ou 3,1 mmol/L (50,4 mg/dL ou 55,8 mg/dL) se expressado como glicose plasmática) do que com insulina NPH, enquanto nenhuma diferença foi observada no diabetes tipo 2.
Em estudos em longo prazo (≥ 6 meses) em pacientes com diabetes tipo 1 recebendo uma terapia com insulina basal- bolus , a glicose plasmática em jejum foi melhorada com Insulina Detemir em comparação com insulina NPH. O controle glicêmico (HbA 1c ) com Insulina Detemir é comparável ao da insulina NPH, com um menor risco de hipoglicemia noturna e sem ganho de peso associado.
Foi observado o desenvolvimento de anticorpos com o uso Insulina Detemir. No entanto, este não parece causar qualquer impacto sobre o controle glicêmico.
Acima de 2 anos
A eficácia e segurança Insulina Detemir foram estudadas por mais de 12 meses em 2 estudos randomizados controlados, em adolescentes e em crianças com diabetes tipo 1 com mais de 2 anos de idade (n=694 expostos no total, Estudos NN304-1689 e NN304-1379). Os dois estudos demonstraram que o controle glicêmico (HbA 1c ) com e Insulina Detemir é comparável ao da insulina NPH quando administrado como terapia basal- bolus : diferença média estimada na HbA 1c e Insulina Detemir-NPH foi de 0,12 (-0,12; 0,36) IC de 95% n= 339 no NN304-1689 e 0,09 (-0,12;0,29) IC de 95% n = 347 no NN304-1379.
Nos dois estudos, o índice de hipoglicemia noturna foi menor para e Insulina Detemir, razão de proporção ajustada e Insulina Detemir/NPH = 0,62 (0,47;0,84) p=0,002 n=347 (NN304-1689) e risco relativo e Insulina Detemir/NPH= 0,74 (0,55; 0,99) IC de 95% p = 0,041 n = 347 (NN304-1379). Menor ganho de peso foi observado com e Insulina Detemir do que com insulina NPH: desvio padrão de peso, e Insulina Detemir-NPH foi -0,15 (-0,23; -0,07) IC de 95% p<0,01 n = 347 (NN304-1689); diferença estimada na alteração média no IMC e Insulina Detemir-NPH = -0,45Kg/m2 (- 0,65; -0,25) IC de 95% p<0,001 n=335 (NN304-1379). O desenvolvimento de anticorpos foi observado com o uso Insulina Detemir. O Estudo NN304-1689 foi prolongado por mais 12 meses (total de dados de tratamento de 24 meses, Estudo NN304-1690) para se avaliar a formação de anticorpos após tratamento em longo prazo com e Insulina Detemir. Os anticorpos médios contra insulina observados aumentaram durante aproximadamente a primeira metade do primeiro ano de tratamento e diminuíram durante o ano e meio restantes do estudo. Os resultados indicam que o desenvolvimento de anticorpos não exerceu efeito negativo sobre o controle glicêmico e a dose de Insulina Detemir.
Insulina Detemir em combinação com liraglutida e metformina
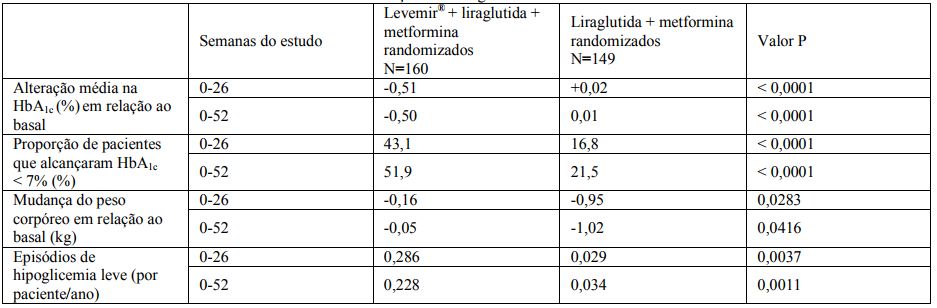
Um estudo randomizado aberto em pacientes com diabetes tipo 2 que não atingiram o objetivo com antidiabéticos orais foi conduzido. O estudo teve início com 12 semanas de liraglutida+metformina, onde 61% alcançaram HbA 1c <7%. Os 39% dos pacientes que não atingiram a meta foram randomizados para utilizar Insulina Detemir uma vez ao dia ou continuar com liraglutida+metformina por 52 semanas. A adição de Insulina Detemir causou uma redução na HbA 1c de 7,6% para 7,1% após 52 semanas. Não houve episódios hipoglicêmicos graves. Ao adicionar Insulina Detemir à liraglutida, o benefício em relação ao peso foi sustentado, veja Tabela 2.
Tabela 2. Dados de estudos clínicos - Insulina Detemir em combinação com liraglutida+metformina
Gravidez
Em um estudo clínico controlado randomizado, mulheres grávidas com diabetes tipo 1 (n=310) foram tratadas com um regime basal-bolus onde Insulina Detemir (n=152) foi comparado com insulina NPH (n=158) com insulina asparte como insulina prandial.
Insulina Detemir mostrou ser não inferior à insulina NPH como medido pela HbA 1c na semana 36 da gestação. O desenvolvimento da HbA 1c média durante a gravidez foi similar para pacientes dos grupos Insulina Detemir e insulina NPH.
A meta de HbA 1c ≤ 6,0% nas semanas 24 e 36 da gestação foi alcançada por 41% do pacientes do grupo Insulina Detemir e por 32% no grupo da insulina NPH.
Nas semanas 24 e 36 da gestação, a glicemia de jejum média foi menor, de forma estatisticamente significativa, no grupo Insulina Detemir do que no grupo de insulina NPH.
Não houve diferença estatisticamente significativa entre os grupos tratados com Insulina Detemir e insulina NPH na taxa de episódios de hipoglicemia durante a gravidez.
As frequências globais de eventos adversos maternos durante a gravidez foram similares nos grupos tratados com Insulina Detemir e insulina NPH; no entanto, uma frequência numericamente mais alta de eventos adversos sérios durante a gravidez em mães (61 (40%) versus 49 (31%)) e no bebê durante a gravidez e após o nascimento (36 (24%) versus 32 (20%)) foi vista em Insulina Detemir comparado com insulina NPH.
O número de crianças nascidas vivas de mulheres que engravidaram após a randomização foi 50 (83%) para Insulina Detemir e 55 (89%) para insulina NPH.
A incidência de pré-eclâmpsia foi de 10.5% (16 casos) e 7.0% (11 casos) nos grupos de Insulina Detemir e insulina NPH, respectivamente. A frequência de crianças com malformações congênitas foi 4 (5%) para o grupo de Insulina Detemir e 11 (7%) no grupo de insulina NPH. Destas, 3 (4%) das crianças do grupo de Insulina Detemir e 3 (2%) crianças do grupo de insulina NPH tiveram malformações graves.
Em aproximadamente um quarto dos bebês, Insulina Detemir foi detectado no sangue do cordão-umbilical em níveis acima do nível inferior de quantificação (<25 pmol/L).
Características farmacológicas
Propriedades Farmacodinâmicas
Mecanismo de Ação
Insulina Detemir é um análogo de insulina basal solúvel de longa ação com uma duração de efeito prolongada e usada como uma insulina basal. O perfil de tempo de ação de Insulina Detemir é significantemente menos variável que o da insulina NPH e insulina glargina (Tabela 3).
Tabela 3. Variabilidade intraindividual do perfil do tempo de ação da Insulina Detemir, insulina NPH e insulina glargina

A ação prolongada de Insulina Detemir é mediada pela forte auto-associação das moléculas de Insulina Detemir no local da injeção e ligação de albumina pela cadeia lateral de ácido graxo. A Insulina Detemir é mais vagarosamente distribuída para tecidos periféricos alvos comparado com insulina NPH. Esses mecanismos combinados de protração fornecem um perfil de ação e absorção mais reprodutível Insulina Detemir comparado com insulina NPH.

Figura 1. Perfil de atividade de Insulina Detemir em pacientes com diabetes tipo 1
A duração de ação é de até 24 horas dependendo da dose, proporcionando a possibilidade de administração de uma ou duas vezes ao dia. Se for administrada duas vezes ao dia, o estado de equilíbrio ocorrerá após 2-3 administrações de dose. Para doses no intervalo de 0,2 - 0,4 U/kg, e Insulina Detemir exerce mais de 50% de seu efeito máximo a partir de 3-4 horas e até aproximadamente 14 horas após a administração da dose.
A proporcionalidade de dose em resposta farmacodinâmica (efeito máximo, duração de ação, efeito total) é observada após administração subcutânea.
Propriedades Farmacocinéticas
Absorção
A concentração sérica máxima é alcançada entre 6 e 8 horas após administração.
Quando administrada duas vezes ao dia, as concentrações séricas do estado de equilíbrio são alcançadas após 2-3 administrações de dose.
A variação intrapaciente na absorção é mais baixa em e Insulina Detemir que em outras preparações de insulina basal.
Distribuição
Um volume aparente de distribuição para e Insulina Detemir (aproximadamente 0,1 L/kg) indica que uma fração alta de Insulina Detemir está circulando no sangue.
Os resultados dos estudos in vitro e in vivo de ligação de proteína demonstram que não há nenhuma interação clinicamente relevante entre Insulina Detemir e ácidos graxos ou outros medicamentos ligados à proteína.
Metabolismo
A degradação Insulina Detemir é similar a da insulina humana; todos os metabólitos formados são inativos.
Eliminação
A meia-vida depois da administração subcutânea é determinada pela taxa de absorção do tecido subcutâneo.
A meia-vida fica entre 5 e 7 horas dependendo da dose.
Linearidade
A proporcionalidade de dose em concentrações séricas (concentração máxima, extensão de absorção) é observada após administração subcutânea na faixa da dose terapêutica.
Não há nenhuma diferença clinicamente relevante entre os sexos nas propriedades farmacocinéticas Insulina Detemir.
Nenhuma interação farmacocinética ou farmacodinâmica foi observada entre a liraglutida e Insulina Detemirquando administrada uma dose única de Insulina Detemir 0,5 U/kg com liraglutida 1,8 mg no estado de equilíbrio em pacientes com diabetes tipo 2.
População especial
As propriedades farmacocinéticas Insulina Detemir foram investigadas em crianças (6-12 anos) e adolescentes (13-17 anos) e comparadas com as de adultos com diabetes tipo 1. Não houve nenhuma diferença nas propriedades farmacocinéticas.
Não houve nenhuma diferença clinicamente relevante na farmacocinética Insulina Detemir entre pessoas jovens e idosas ou entre pessoas com insuficiência renal ou hepática e pessoas saudáveis.
Dados de segurança pré-clínicos
Testes in vitro em linhagens celulares humanas que investigaram a ligação aos receptores de insulina e de IGF-1 mostraram que a Insulina Detemir tem uma afinidade reduzida para ambos receptores, assim como um efeito reduzido no crescimento de células comparado à insulina humana.
Dados não clínicos não revelaram nenhum risco especial para seres humanos com base em estudos convencionais de farmacologia de segurança, toxicidade de dose repetida, genotoxicidade, potencial carcinogênico e toxicidade para reprodução.
Como devo armazenar o Levemir?
Antes de aberto, Levemir ® FlexPen ® que não está sendo utilizado deve ser armazenado em refrigerador (temperatura entre 2 ºC e 8 ºC), distante do compartimento do congelador. Não congelar.
Em uso ou carregado como reserva, armazenar em temperatura ambiente, abaixo de 30 °C ou sob refrigeração entre 2 °C e 8 °C, distante do compartimento do congelador, por no máximo 6 semanas (42 dias). Não congelar.
Levemir ® deve ser descartado 42 dias após ter sido inicialmente colocado em uso, mesmo que ainda tenha produto no carpule.
Sempre mantenha Levemir tampado quando não estiver em uso para protegê-lo da luz.
Levemir ® deve ser mantido longe do calor excessivo e luz direta.
Transporte
O transporte do medicamento deverá ser realizado através de uma embalagem que proporcione proteção térmica e evite alteração brusca de temperatura, incidência de luz direta e vibração excessiva. No caso de viagens aéreas, não despachar o produto dentro das malas. O compartimento de bagagem dos aviões atinge temperaturas muito baixas, podendo congelar o medicamento.
Descarte
O descarte de agulhas deve ser realizado através de embalagens coletoras resistentes, como latas e plásticos, para eliminar o risco de acidentes e contaminação. As embalagens coletoras contendo as agulhas e os medicamentos usados, vencidos ou fora de uso, assim como seu sistema de aplicação devem ser descartados em Postos de Coleta localizados em Farmácias, Drogarias, Postos de Saúde ou Hospitais, que possuem coletores apropriados. O cartucho e a bula, feitos de papel e que não possuem contato direto com o medicamento, podem ser descartados no lixo reciclável. Em caso de dúvidas consulte seu farmacêutico, enfermeiro, médico ou vigilância sanitária.
Exclusivo Levemir ® FlexPen ® : Não tente repor o conteúdo do sistema de aplicação ou reutilizá-lo. Uma vez vazio, ele deve ser descartado.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Número de lote e datas de fabricação e validade: vide embalagem.
Características do medicamento
Levemir ® é uma solução injetável aquosa, com aspecto límpido e incolor.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais do Levemir
Registro MS 1.1766.0019
Farmacêutico responsável
Luciane M. H. Fernandes
CRF/PR nº 6002
Fabricado por
Novo Nordisk A/S
DK-2880 Bagsvaerd, Dinamarca
Ou
Novo Nordisk A/S
DK-4400 Kalundborg, Dinamarca
Ou
Novo Nordisk Production SAS
Chartres, França
(vide cartucho)
Importado por
Novo Nordisk Farmacêutica do Brasil Ltda.
Rua Francisco Muñoz Madrid, 625
São José dos Pinhais/PR
Ou
Fabricado por
Novo Nordisk Produção Farmacêutica do Brasil Ltda.
Montes Claros/MG
Registrado e comercializado por
Novo Nordisk Farmacêutica do Brasil Ltda.
Rua Professor Francisco Ribeiro, 683
Araucária/PR
CNPJ: 82.277.955/0001-55
Indústria Brasileira
(vide cartucho)
SAC:
0800 14 44 88
Venda sob prescrição médica.










